
题目列表(包括答案和解析)
25、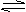 (6分)一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:(1)此反应的化学方程式中
(6分)一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:(1)此反应的化学方程式中 =__________
=__________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:_________________________
 (3)下列叙述中能说明上述反应达到平衡状态的是_______________
(3)下列叙述中能说明上述反应达到平衡状态的是_______________
A.反应中M与N的物质的量之比为1︰1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
24、(8分)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子最外层电子数与次外层电子数之比为3∶4; Z、X处于同一主族;X与N形成的化合物XN常温下为气体。据此回答:
(1)M、N的最高价氧化物的水化物中酸性较强的是(写出化学式)
(2)Z与M可形成常见固体化合物C,用电子式表示C 。
(3)已知通常状况下1g X2在Y2中完全燃烧生成液态的X2Y时放出a kJ的热量,请写出其热化学方程式 。
(4)X与Y、X与M均可形成18电子分子,写出这两种分子在水溶液中反应生成一种单质和一种10电子分子的化学方程式 。
23、(8分)某学生课外活动小组利用右图所示装置分别做如下实验:
 ⑴在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是:________
_______
_______________。
⑴在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________________溶液;加热时溶液由红色逐渐变浅的原因是:________
_______
_______________。
⑵在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复
无色,则此溶液可能是________________溶液;加热时溶液由无色变
为红色的原因是: ____________________________________。
22、(4分)在试管里放入一块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。
(1)若铜片还有剩余,硫酸________消耗完毕(填“已经”或“没有”)。其理由是________
____________________________________________________________________________。
(2)往上述试管中加入以下物质会使铜的质量进一步减少的是_____________________。
A、KNO3 B、氨水 C、FeCl2 D、FeCl3
21、 (4分)某简单微粒的结构示意图为:
(4分)某简单微粒的结构示意图为:
且X、Y 均为不大于20的正整数,据此回答下列问题:
(1)若该微粒一般情况下不与其它元素的原子反应,这种微粒的符号是
(2)若该微粒有很强的非金属性,且只需得到一个电子就能达到稳定结构,这种微粒的结构示意图为
(3)若该微粒为一价阳离子,且对应的碱为可溶性强碱,则x= y= 。
20、 化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如右图所示。现提供以下化学键的键能:P-P 198kJ·mol-1、P-O 360 kJ·mol-1、氧气分子内氧原子间的键能为498 kJ·mol-1。估算P4+3O2 =P4O6的反应热∆H为
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如右图所示。现提供以下化学键的键能:P-P 198kJ·mol-1、P-O 360 kJ·mol-1、氧气分子内氧原子间的键能为498 kJ·mol-1。估算P4+3O2 =P4O6的反应热∆H为
A.+1638 kJ·mol-1 B.-1638 kJ·mol-1
C.-126 kJ·mol-1 D.+126 kJ·mol-1
19、铊(Tl)是某超导材料的组成元素之一,与铝同一主族,位于第6周期。Tl 3+ 与Ag在酸性介质中发生反应:Tl 3++2Ag===Tl + +2Ag +。根据信息下列推断不正确的是
A.Tl + 的最外层有1个电子 B.Tl 3+ 的氧化性比Al 3+强
C.Tl能形成+3价和+1价的化合物 D.Tl + 的还原性比Ag弱
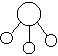
18、已知E与G反应生成L和M,且组成E、G、L、M分子的元素原子序数均小于10,用它们的结构式表示反应如下图所示。则下列判断错误的是
 +
+ 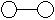

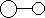 +
+ 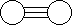
E G L M
A.G是最活泼的非金属单质 B.L分子中有共价键
C.E能使紫色石蕊试液变蓝色 D.M化学性质很活泼
17、已知镁和稀硝酸反应时,每有1mol HNO3反应,就有0.8mol电子转移,此时硝酸的还原产物可能是
A.NO2 B.N2O C.N2 D.NO
16、已知碱能吸收氮氧化物(NO不能与碱反应):2NO2 + 2NaOH =NaNO2 +NaNO3+ H2O,
NO + NO2 + 2NaOH = 2NaNO2 + H2O,根据上述反应原理,下列气体理论上能被过量NaOH溶液全部吸收的是
A.2mol O2和4molNO2 B.1molO2 和4molNO
C.2molNO D.4molNO和1molNO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com