
题目列表(包括答案和解析)
9.下列有关叙述中能说明M比N的非金属性强的叙述是( )
①非金属单质M能从N的化合物中置换出非金属单质N
②M原子比N原子容易得到电子
③单质M跟H2反应比N跟H2反应容易得多
④气态氢化物水溶液的酸性HmM>HnN
⑤氧化物水化物的酸性HmMOx>HnNOy
⑥熔点M>N
A.①②③ B.②⑤ C.①②③④⑤ D.全部
8.根据元素周期律及物质结构的有关知识,下列有关比较错误的是( )
A.离子半径:S2->Cl->Ca2+ B.原子半径:Ca>S>Cl
C.热稳定性:HCl>H2S>H2Se D.还原性:H2S>H2Se>H2Te
7.下列对物质用途的描述中,错误的是( )
A.臭氧可用于漂白和消毒
B.Cl2、SO2、NaClO 均可用于漂白某些物质
C.浓硫酸具有吸水性,可用于干澡HCl、H2S、O2
D.过氧化氢可用作氧化剂、漂白剂、消毒剂和脱氯剂
6.下列说法中,不正确的是 ( )
A.硫既可作氧化剂,也可作还原剂 B.二氧化硫既具有氧化性也具有还原性
C.可以用铁罐贮运冷的浓硫酸 D.稀硫酸不与铁反应
5.Z元素的某同位素离子Zn-,其核外共有X个电子,该同位素原子的质量数为A。则其原子核内含有的中子数为 ( )
A.A-X+n B.A-X-n C.A+X+n D.A+X-n
4.设NA代表阿伏加德罗常数,下列说法正确的是( )
A.18克2H2O(重水)中所含电子数为2NA
B.1molNa2O2中含有4NA个离子
C.在标准状况下,11.2LSO3所含原子的数目为4NA
D.100ml浓度为12mol/L的浓硫酸中含H+的数目少于2.4NA
3.下列各组物质中,互为同位素的是( )
A.石墨、金刚石 B.氕、氘 C.纯碱、烧碱 D.水、重水
2.下列化学用语表达正确的是( )
A.次氯酸的结构式:H一Cl一O B.碳-12 的原子符号: C
C
C.Mg原子结构示意图: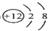 D.过氧化氢的电子式H+ [:O:O:]2- H+
D.过氧化氢的电子式H+ [:O:O:]2- H+
1.你认为减少酸雨产生的途径可采取的措施( )
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰
⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
21、(15分)成都市某中学高一课外兴趣小组为探究铜跟硫酸的反应情况,设计了如图所示装置进行有关实验。
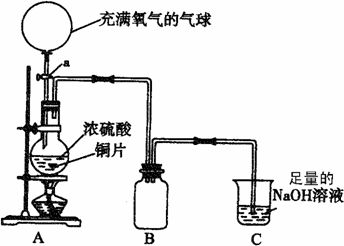
(1)先关闭活塞a,将6.4g铜片和12 mL某浓度的浓硫酸放在圆底烧瓶中共热至反应完毕,发现烧瓶中还有铜片剩余。再打开活塞a,将气球中的氧气缓缓挤入圆底烧瓶,最后铜片完全消失。
①写出上述过程中烧瓶内发生的化学方程式: ;
②B是用来收集实验中产生的气体的装置,但导管未画全,请在上图中把导管补充完整;
③实验结束后,装置C中的溶液中可能含有的溶质有 。
(2)该小组甲同学对“如何检验SO2中混有少许CO2”这个问题很感兴趣,他将A中铜片换作木炭粉,并在A、B之间连接了如下装置:

试剂:a. NaOH溶液 b. 品红溶液 c. 酸性KMnO4溶液 d. Ba(OH)2溶液
请回答:①该同学的实验装置A中发生的化学方程式 。
②若要达到此目的,可以在:(填所提供试剂编号)
D中加入 ;E中加入 ;F中加入 。
(3)事实证实,第(1)问铜片完全消失后,硫酸仍有剩余,乙同学欲测定余酸的物质的量浓度,假设反应前后溶液体积变化忽略不计,他向反应后溶液中加入含溶质a mol的NaOH溶液刚好使溶液中Cu2+全部沉淀。据此,他能求出余酸的物质的量浓度吗?若能,请写出余酸物质的量浓度的计算式:= mol/L(用含a的代数式表达,若不能,该空不填)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com