
题目列表(包括答案和解析)
6.下列微粒中,与铵离子的质子数和电子数都相等的是( )
A.OH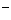 B.H
B.H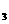 O
O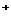 C.NO D.HF
C.NO D.HF
5.同一周期中,X、Y、Z三种元素,其气态氢化物稳定性按X、Y、Z的顺序不断增强,下列说法正确的是( )
A.非金属性X>Y>Z
B.原子半径X>Y>Z
C.它们氧化物水化物的酸性按X、Y、Z顺序增强
D.气态氢化物的还原性按X、Y、Z顺序增强
4.元素X原子的最外层有3个电子,元素Y原子的最外层有6个电子,这两种元素形成的化合物的化学式可能是( )
A.XY2 B.X2Y3 C.X3Y2 D.X2Y
3.下列说法中正确的是( )。
A.同主族元素的原子半径,随着原子序数的递增而减小
B.短周期元素中最外层电子数等于电子层数的元素有2种
C.质量数表示同位素相对原子质量的近似值
D.核外电子排布相同的微粒,一定具有相同的化学性质
2. 张青莲是我国著名的化学家。1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值。这是原子量表中的首次采用我国测定的原子量值。已知In的原子结构如图所示,则下列关于In的说法不正确的是
张青莲是我国著名的化学家。1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值。这是原子量表中的首次采用我国测定的原子量值。已知In的原子结构如图所示,则下列关于In的说法不正确的是
A.In为长周期元素
B.In为过渡元素
C.In易导电导热
D.In在反应中容易失电子
1. 1995年我国科研人员在兰州首次合成了镤元素的一种同位素镤–239,并测知其原子核内有148个中子。现有A元素的一种同位素,比镤–239的原子核内少54个质子和100个中子,则A元素在元素周期表中的位置是
A.第3周期第IA族 B.第4周期第IA族
C.第5周期第IA族 D.第3周期第IIA族
23.(8分)把32.5g的锌投入到50mL18mol/L的浓硫酸中,锌完全消耗后,收集到的气体平均相对分子质量为33,试计算:
(1)收集到的气体在标准状况下的体积是_____________升?
(2)反应后溶液中氢离子的物质的量浓度是_____________mol/L
(3)向上述反应后的溶液中逐滴加入2.6mol/LBaCl2溶液,此时沉淀刚好完全,求所
加入的BaCl2溶液的体积是多少毫升?(请写出该问的具体计算过程)
南充高中2008-2009学年度下学期期中考试
22.(4分)在标准状况下,臭氧发生器中装入500 mL氧气,通电一段时间后,气体的体积变为475ml,求氧气的转化率是多少?
21.(7分)甲、乙、丙为短周期元素形成的常见单质,甲、乙同周期,乙、丙同主族,C、D、E、F、G均为常见的化合物。B、X的式量相同,E的式量比D大16,在一定条件下各物质之间相互转化关系如图所示:(其中B和H2O反应生成丙和C)
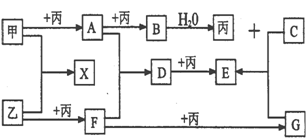
(1)B的电子式是_______________
(2)上述物质A、B、C、E、F、G中能与水发生反应且在反应中既不作氧化剂也不作还原剂的物质是___________________。(用化学式表示)
(3)反应D与丙反应的化学方程式是_____________________________。
(4)在X与D的混合液中加入稀硫酸有浅黄色沉淀产生,写出该反应的离子方程式是______________________________
20.(9分)某学习小组对教材实验“在200 mL烧杯中放入20g蔗搪(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究.
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味。压缩“黑色面包”时,感觉较硬,放在水中呈漂浮状态。同学们由上述现象推测出下列结论:
①浓硫酸具有酸性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有强氧化性 ⑤浓硫酸具有强氧化性糖炭化得到的碳连成整体,碳原子间形成了化学键 ⑥黑色物质具有强吸附性
其中依据充分的是________________(填序号)
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:

试回答下列问题:
① 上图A中应选用下列装置_____________(填编号)。

② B装置所装试剂是________;D装置的作用是___________;E装置所装试剂是_________________
③ A 装置中使蔗糖变黑的化学反应方程式为_________________________
④ 如果反应中有一氧化碳气体产生,则F装置中的现象为__________________
其反应的离子方程式是______________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com