
题目列表(包括答案和解析)
20.(10分)已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如下转化关系
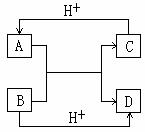
(1)如果A、B、C、D均是10电子的粒子,请写出:
C的化学式_______________________;D的电子式______________________.
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A与B在溶液中反应的离子方程式______________.
②根据上述离子方程式,可以判断C与B结合质子(H+)的能力大小是(用化学式或离子符号表示):________>________.
19.(10分)有A、B、C、D四种元素,其中A、B、C为短周期元素,A元素的周期数、主族数、原子序数均相同,BO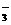 含有32个电子,C元素的原子最外层电子数比次外层电子数少2个,C的阴离子与D的阳离子具有相同的电子层结构,C和D可形成化合物D2C,试回答下列问题:
含有32个电子,C元素的原子最外层电子数比次外层电子数少2个,C的阴离子与D的阳离子具有相同的电子层结构,C和D可形成化合物D2C,试回答下列问题:
(1)A、B、C、D四种元素的符号分别是_________、_________、__________、__________.
(2)A、B、C可形成两种既含离子键又含共价键的化合物,分别为___________和___________.(写化学式)
(3)D2C形成过程的电子式表示为_________________________________________________.
18.下列说法正确的是( )
A.核外电子总数相同的原子,一定是同种元素的原子
B.ⅥA族元素的原子,其半径越大,越容易得到电子
C.任何条件下,零族元素的单质都是气体
D.所有主族元素的原子,形成单原子离子时的化合价和它的族序数相等
请将选择题答案填入下表
第Ⅱ卷(非选择题,共46分)
(本大题包括5小题)
17.X、Y是元素周期表ⅦA族中的两种元素,下列叙述中能说明X的非金属性比Y强的是( )
A.X原子的电子层数比Y原子的电子层数多
B.X的氢化物的沸点比Y的氢化物的沸点低
C.X的气态氢化物比Y的气态氢化物稳定
D.Y的单质能将X从NaX的溶液中置换出来
16.元素X的一种同位数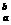 X,元素Y的一种同位素
X,元素Y的一种同位素 Y,已知a>c,b>d,则元素X和Y的相对原子质量的大小关系是( )
Y,已知a>c,b>d,则元素X和Y的相对原子质量的大小关系是( )
A.M(X)>M(Y) B.M(X)<M(Y) C.M(X)=M(Y) D.不能确定
15.具有相同电子层结构的三种粒子An+、Bn-、C,下列分析正确的是( )
A.原子序数关系是C>B>A B.粒子半径关系是An+>Bn-
C.C一定是惰性元素的一种原子 D.原子半径关系是A<C<B
14.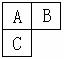 A、B、C三种短周期元素在周期表中的位置如图所示。已知A、C可分别与B形成化合物X和Y,A与B的质子数之和为C的质子数,现有以下说法,其中判断正确的组合为( )
A、B、C三种短周期元素在周期表中的位置如图所示。已知A、C可分别与B形成化合物X和Y,A与B的质子数之和为C的质子数,现有以下说法,其中判断正确的组合为( )
①B与C均存在同素异形体 ②X的种类比Y的多
③常温下,B的氢化物中无H+ ④C的最高价氧化物对应的水化物能与A的氢化物形成三种盐
A.①②③④ B.②④ C.①②④ D.①②
13.a、b、c、d是四种短周期元素,a、b、d同周期,c、d同主族,a的原子结构示意图为
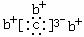
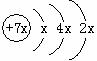 ,b与c形成的化合物的电子式为:
,则下列比较正确的是(
)
,b与c形成的化合物的电子式为:
,则下列比较正确的是(
)
A.原子半径a>c>b B.原子的氧化性a>c>d
C.离子半径b+>c3―>d3― D.最高价含氧酸的酸性c>d>a
12.下列叙述正确的是( )
A.同一主族的元素,原子半径越大,其单质的熔点一定越高
B.同一周期元素的原子,半径越小越容易失去电子
C.同一主族的元素的氢化物,相对分子质量越大,它的沸点一定越高
D.稀有气体元素的原子序数越大,其单质的沸点一定越高
11.下列说法中正确的是( )
A.最外层电子数为次外层电子数一半的元素一定属于碱金属元素
B.元素周期表中从ⅢB族到ⅡB族之间的10个纵行的元素都是金属元素
C.第ⅡA族与第ⅢA族元素的原子序数一定相差1或11
D.若主族元素的族序数为a,周期数为b,当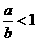 时,该元素为非金属元素
时,该元素为非金属元素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com