
题目列表(包括答案和解析)
23. 短周期主族元素R的族序数是其周期序数的2倍,R在其最高价氧化物中的质量分数约为27.30/0。已知R原子核内的质子数与中子数相等。试通过计算:
(1)确定R是什么元素?
(2)确定R元素在周期表中的位置
(3)最高价氧化物的化学式是什么?并书写最高价氧化物的电子式
养正中学2008~2009学年第二学期化学第一次月考答题卡
22.喷泉是一种常见的自然现象,其产生原因是存在压强差。
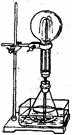
 (1)右上图为化学教学中用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
(1)右上图为化学教学中用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是
A.HCl和H2O B.O2和H2O C.NH3和H2O D.CO2和NaOH溶液
(2)某学生积极思考产生喷泉的其他办法,并设计了如右下图所示的装置。
①在锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NH4HCO3与稀盐酸
②在右下图锥形瓶外有一水槽,瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是
 A.浓硫酸 B.食盐 C.硝酸钾 D.硫酸铜
A.浓硫酸 B.食盐 C.硝酸钾 D.硫酸铜
这种方法产生喷泉的原理是
③比较右上图和右下图两套装置,从产生喷泉的原理来分析,右上图是 上部烧瓶内气体压强;右下图是 下部锥形瓶内气体压强。
(3)常见的人造喷泉及火山爆发的原理与上述 (填右上图或右下图)装置的原理相似。
21.(11分) A、B、C为短周期元素,在周期表中所处位置如下图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
 (1)写出A、B、C三种元素的名称
、 、
。
(1)写出A、B、C三种元素的名称
、 、
。
(2)B位于元素周期表第 周期,第 族。
(3)C的原子结构示意图为 。
(4)比较B、C的的原子半径,B C,写出A的气态氢化物与B的最高价氧
化物的水化物反应的化学方程式
(5)A的单质的电子式为 ,其中的化学键属于 键(填“离子”或“共价”)。
1.现20.现有下列短周期元素性质的数据:(8分)
|
编号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径/10-10m |
1.10 |
0.99 |
1.86 |
0.66 |
0.88 |
0.70 |
1.52 |
1.60 |
|
最高化合价 和最低化合价 |
+5 -3 |
+7 |
+1 |
-2 |
+3 |
-3 |
+1 |
+2 |
请确请确定以上8种元素在周期表中的位置,将元素的编号填入下表中:
|
族 周期 |
ⅠA |
ⅡA |
|
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
|
1 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
19.(12分)下表是周期表中的一部分,根据A-N在周期表中的位置,按要求回答下列问题:(用相关的元素符号或分子式表示)
 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
1 |
A |
|
|
|
|
|
|
|
|
2 |
|
|
|
B |
C |
|
D |
E |
|
3 |
F |
G |
H |
I |
J |
K |
M |
|
(1)表中元素,只有负价而无正价的元素是 ,氧化性最强的单质是 ,化学性质最不活泼的元素是________,金属性最强的单质与水反应的化学方程式是____________________________________。
(2) 最高价氧化物的水化物酸性最强的是 ___________ ,呈两性的是 ;
(3)元素F形成的稳定的氧化物在呼吸面具中供氧时的化学方程式是 ,该化合物的焰色为_________色。
(4)元素M的单质和石灰乳作用可制成有漂白和消毒作用的漂白粉, 用化学方程式表示漂白粉在潮湿空气中起漂白作用的原理
18.已知反应的化学方程式aFeCl2+bKNO3+cHCl dFeCl3+gKCl+fX+eH2O,若b=1,a=3, X为生成物,其化学式应为 ( )
dFeCl3+gKCl+fX+eH2O,若b=1,a=3, X为生成物,其化学式应为 ( )
A.N2 B.NH4Cl C.NO D.NO2
第Ⅱ卷 (非选择题共46分)
17.已知X元素原子的L电子层比Y元素原子的L电子层少3个电子,Y元素原子核外总电子数比X元素总电子数多5个,则X、Y可形成( )
A.离子化合物Y( XO3)2 B. 离子化合物Y2X3
C. 共价化合物Y3X2 D. 共价化合物XY2
16.盛有氯化钡稀溶液甲乙两试管分别通入SO2至饱和,若向甲试管中加入足量硝酸,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是 ( )
A.甲、乙两试管都有白色沉淀生成
B.甲、乙两试管都没有白色沉淀生成
C.甲试管没有白色沉淀生成而乙试管有
D.甲试管有白色沉淀生成而乙试管没有
15.1999年曾报导合成和分离了含能量的正离子N5+的化合物N5AsF6,下列错误的是( )
A.N5+共有34个核外电子 B.N5+中氮原子之间以共用电子对结合
C.化合物N5AsF6中As化合价为+1 D.化合物N5AsF6中F化合价为-1
14.把含硫酸铵和硝酸铵的混合液a L分成两等份。一份加入bmol NaOH并加热,恰好把NH3全部赶出;另一份需消耗cmol BaCl2沉淀反应恰好完全,则原溶液中NO3- 的浓度为 ( )
A .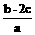 B .
B . 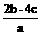 C.
C.
 D
.
D
.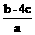
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com