
题目列表(包括答案和解析)
6.下列关于钠、钾、铷、铯的叙述中不正确的是
A.与H2O反应最剧烈的是Cs B.与氧气反应时均生成单一的氧化物
C.原子半径随核电荷数的增大而增大D.单质的熔沸点随核电荷数的增大而降低
5.氧化还原反应的实质是
A.分子中的原子重新组合 B.氧元素的得失
C.电子的得火或共阴电子对的偏移D.化合价的改变
4.下列物质中,属于纯净物的是
A.液氯 B.氯水 C.漂粉精 D.盐酸
3.下列标记,不需要在容量瓶上标有的是
A.标线 B.温度 C.浓度 D.容量
2.下列物质不属于化石燃料的是
A.煤 B.石油 C.氢气 D.天然气
1.下列科学家中,为我国化学工业做出重大贡献的是
A.邓稼先 B.侯德榜 C.李四光 D.华罗庚
26.将5.00g氯化钠、溴化钠和氯化钙的混和物溶于水,通入足量Cl2充分反应,然后把溶液蒸干并灼烧(高温加热),灼烧后残留物的质量为4.914g。若将此残留物再溶于水加入足量的碳酸钠溶液,所得的沉淀经干燥后质量为0.270g。求混和物中各化合物的质量分数。
25.(8分)已知漂白粉与浓盐酸反应产生氯气,某同学欲通过如下装置测定由此产生氯气的体积并验证干燥纯净的氯气无漂白性。回答下列问题:
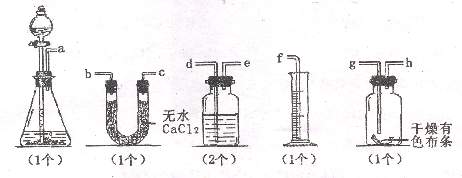
(1)请用字母填写装置的连接顺序:
a接( )、( )接( )、( )接( )、( )接( )、( )接( );
(2)两个洗气瓶中所装的液体分别是_____________、______________;
(3)在制取氯气前,必须进行的一项操作的步骤是_________________;
(4)某同学在实验中,发现量筒中未收集到液体,则失败的原因可能是
___________________________________________________________。
4.(8分)欲用密度为1.18g/cm3(质量分数36.5%)的浓盐酸配制250ml,1mol/L盐酸,回答下列各问;
(1)所需浓盐酸体积约为_____________mL(填整数);
(2)所需仪器为_______________________________________________________________;
(3)若定容时俯视,所配溶液的物质的量浓度比要配制的溶液的______(填“偏高”或“偏低”);
(4)若定容后再摇匀静置,发现凹液面低于刻度线。此时(填标号)_______。
A.可直接转移到试剂瓶中
B.应加水重新定容后贮存于容量瓶中
C.应重新定容后再转移到试剂瓶中
23.(12分)右图所涉及的物质均为中学化
学中的常见物质,其中C、D、E为单质,其
余为化合物。它们存在如图的转化关系,反
应中生成的水及次要产物均已略去。
(1)写出化学式:B___________、E___________;
(2)指出MnO2在相关反应中的作用:在反应①中是________剂,在反应②中是________剂;
(3)写出B→D反应的离子方程式:____________________________________________;
(4)写出变化③的离子方程式:____________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com