
题目列表(包括答案和解析)
27、下图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置,请回答下列问题:
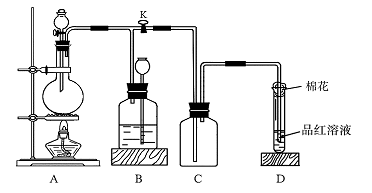
Ⅰ.(1)在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,烧瓶中反应的化学方程式为:_____ 。
(2)装置D中试管口放置的棉花中应浸有一种液体,这种液体是 ,
其作用是: 。
(3)装置B的作用是贮存多余的二氧化硫和防止其污染环境,则B中应盛放的液体是(填写字母代号)________;
a.水 b.浓溴水; c.KMnO4酸性溶液 d.NaHSO3饱和溶液
Ⅱ.两位同学设计了下述两个方案,并都认为如果观察到的现象和自己设计的方案一致,即可确证无色混合气体中含有CO2和SO2
方案甲:无色气体 → 酸性KMnO4溶液 → 澄清石灰水
(褪色) (浑浊)
方案乙:无色气体 → 足量品红溶液 → 澄清石灰水
(颜色变浅) (浑浊)
试评价上述各方案是否严密,并说明理由(如果严密,则不用回答理由一问)
方案甲 (填“严密”或“不严密”),理由: 。
方案乙 (填“严密”或“不严密”),理由: 。
26、(8分)在一定条件下,下列各物质可发生如下图所示的变化(反应中生成的水没有写出),已知A是一种淡黄色的物质,F为主要大气污染物之一。请回答有关问题:
(1)固体A的电子式为___________。
(2)分别写出反应(Ⅰ)、(Ⅱ)的离子方程式:
Ⅰ_________________________________Ⅱ____________________________________。
(3)气体F在一定条件下可被固体A完全吸收,该反应的化学方程式为:
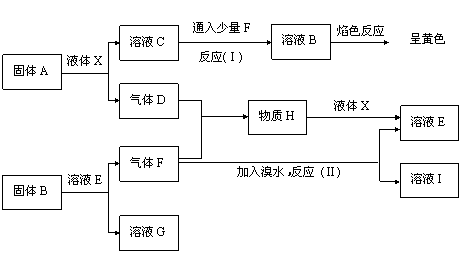 ___________________________________________________________。
___________________________________________________________。
25、(9分)元素A-D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题。
|
元素 |
A |
B |
C |
D |
|
性质 结构 信息 |
单质制成的高压灯,发出的黄光透雾力强、射程远。 |
-2价阴离子具有强还原性 |
单质能用来消毒、制备漂白剂、氯仿等有机溶剂和多种农药。 |
+2价阳离子的核外电子排布与氖原子相同。 |
(1)用电子式表示A和B形成化合物的过程: 。
实验室制备C单质的化学方程式 。
(2)对元素B的单质或化合物描述正确的是 。
a. B元素的最高正价为+6
b. 常温、常压下单质难溶于水
c. 单质分子中可能含有18个电子
d. 在一定条件下D能与单质B反应
(3)B和C两元素非金属性较强的是(写元素符号) 。写出能证明该结论的一个实验事实(用一个化学方程式表示) 。
24、(8分)在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的化学式是 ;X与氢元素形成的化合物的电子式是 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是 ;D与E能形成一种分子,该分子的结构式为 ;
(3)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为 。
23、 (7分)右图是从实验室取出的硫酸试剂标签上的部分内容
(7分)右图是从实验室取出的硫酸试剂标签上的部分内容
(1)该硫酸的物质的量浓度为 。
(2)1mol Zn与足量该硫酸反应产生 g的
气体(填写气体名称)。
(3)该硫酸与等质量的水混合所得到的溶液的物质的量浓度
(填“大于”“小于”“等于”)9.2 mol/L。
22、(6分)A、B两种离子具有相同的电子层,A、B两元素的单质都能与水剧烈反应,在反应中A单质为氧化剂,B单质为还原剂。则:
(1)A离子的结构示意图为____________,B原子的结构示意图为___________。
(2)A单质与水反应的化学方程式为_________ _____。
(3)B单质与水反应的离子方程式为_________ _____。
21、(6分)根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有_______种,金属性最强的元素与氧反应生成的化合物的电子式______________;
(2)属于稀有气体的是_________(填元素符号,下同);
(3)第三周期中,原子半径最大的是(稀有气体除外) ;
(4)推测Si、N最简单氢化物的稳定性_________大于__________(填化学式)。
20、向1mol赤热的Cu2S通入足量的水蒸气,生成2mol H2,则Cu2S应转化成( )
A.Cu和SO2 B.Cu和S C.CuO和SO2 D.CuO和S
Ⅱ卷(非选择题,共60分)
将二卷答案填写在答题纸上,请认真审题,规范书写,祝你成功!
19、根据等电子原理:由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之
和相同,可互称为等电子体,它们具有相似的结构特征。以下各组微粒结构不相似的是( )
A.CO和N2
B.O3和NO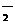 C.N2H4和C2H4 D.CO2和N2O
C.N2H4和C2H4 D.CO2和N2O
18、X是由两种短周期元素构成的离子化合物,1molX含有20mol电子。下列说法中不正确的是( )
A.固体中阳离子和阴离子所含电子数一定相等
B.固体中一定只有离子键没有共价键
C.所含元素一定不在同一周期也不在第一周期
D.固体中阳离子半径一定小于阴离子半径
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com