
题目列表(包括答案和解析)
23.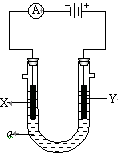 电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液
a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1) 若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在
两边各滴入几滴酚酞试液,则
① 电解池中X极上的电极反应式为 。在X极附近
观察到的现象是 。
② Y电极上的电极反应式为 ,检验该电极反应产物的试剂可以是 。
(2) 如要用电解法精炼粗铜,Y电极为粗铜(含少量锌、碳、金、银等杂质),电解液a选用CuSO4溶液。则X电极的材料是 ,电极反应式是 。
第II卷(选做题,30分)
友情提醒:
本部分试卷分为A、B两类,同学们可以选做A、B两类中任何一类,但选择要统一,不可两类混做,多做或混做均不得分。
A类题
22.(1)将20g Ba(OH)2·8H2O晶体与10 g NH4Cl晶体一起放入小烧杯中,用玻璃棒迅速搅拌,用手触摸烧杯外壁。
①实验中玻璃棒的作用是 。
②写出有关反应的化学方程式 。
③通过手的触感,说明该反应为 (填“吸热”或“放热”)反应,这是由于反应物的总能量 (填“小于”或“大于”)生成物的总能量。
(2)已知键能: N≡N 946KJ/mol, H-H 436KJ/mol, H-N 391KJ/mol。
写出合成氨反应的热化学方程式为
21.下表是元素周期表的一部分,针对表中的①-⑧种元素,填写下列空白。
|
主族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
O |
|
2 |
|
|
|
① |
② |
③ |
|
|
|
3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
(1)在这些元素中,化学性质最不活泼的是______(填元素符号)这种元素的原子结构示意图为_______。
(2)用电子式表示元素⑦的单质分子的形成过程________ ___
(3)在非金属元素的最高价氧化物所对应的水化物中,酸性最强的化合物是________(填化学式)。在金属元素氧化物所对应的水化物中,碱性最强的化合物是_______(填化学式),具有两性的化合物是_______(填化学式)。
(4)元素③的氢化物的电子式为_______。元素③的氢化物分别跟元素④、元素⑦的单质反应的化学方程式是_______________________、 。
20.在下列反应中,生成物能量总和高于反应物能量总和的是
A.Zn(s) + CuSO4(aq) = ZnSO4(aq) + Cu(s) △H =-216kJ•mol-1
B.CaCO3(s) = CaO(s) + CO2(g) △H =+178.5kJ•mol-1
C.2HI(g) = H2(g) + I2(s) △H =-53.0kJ•mol-1
D.H+(aq) + OH-(aq) = H2O(l) △H =-57.2kJ•mol-1
19.与主族元素在周期表中所处的位置有关的是
A.相对原子质量 B.次外层电子数
C.核内中子数 D.电子层数和最外层电子数
18.下列说法正确的是
A.Li是最活泼金属,F是最活泼非金属
B.Mg(OH)2碱性比Ca(OH)2强
C.元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
D.X2+的核外电子数目为18,则X在第四周期第ⅡA族
17.下列各图所表示的反应是吸热反应的是

A B C D
16.可逆反应2SO2 + O2
 2SO3达到平衡的标志是
2SO3达到平衡的标志是
① 消耗2 mol SO2的同时生成2 mol SO3
② SO2、O2与SO3的物质的量之比为2∶1∶2
③ 反应混合物中,SO3的质量分数不再改变
A.①② B.①③ C.只有③ D.只有①
15.用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是
A.不用稀硫酸,改用98%浓硫酸 B.加热
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
14.已知化学能与其他形式的能可以相互转化,下列反应中能量的转化形式主要是由化学能转化为热能的是
A.CH4+2O2  CO2+2H2O
CO2+2H2O
B.CaCO3  CaO+CO2↑
CaO+CO2↑
 C.2H2O
C.2H2O
 2H2↑ + O2↑
2H2↑ + O2↑
D.Pb+PbO2+2H2SO4 2PbSO4+2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com