
题目列表(包括答案和解析)
6.NA为阿伏加德罗常数,下列叙述正确的一组是( )
A.由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2gH2,则电路通过电子0.4NA
B. 18 g D2O中含有的质子数目为10NA
C.1 mol Cl2发生反应时,转移的电子数一定是2 NA
D.常温常压下,16 g O3所含的原子数为NA
5.下列叙述中,正确的是( )
A.离子化合物中不含共价键 B.共价化合物中不含离子键
C.非金属元素组成的化合物一定是共价化合物
D. 两种元素组成的分子中一定只有极性键
4.某主族元素R的最高价与负化合价的代数和为4,下列叙述正确的是( )
A.R的气态氢化物为RH4
B.R一定能形成氧化物为RO2和RO3
C.R为第VI A族元素
D.R的气态氢化物的水溶液一定呈酸性
3.下列化合物中阴离子半径和阳离子半径之比最大的是( )
A.LiI B.NaBr C.KCl D.CsF
2.2007年诺贝尔化学奖得主Gerhard Ertl对金属Pt表面催化CO氧化反应的模型进行了深入研究。下列关于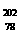 Pt的说法正确的是( )
Pt的说法正确的是( )
A. 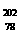 Pt和
Pt和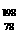 Pt的核外电子数相同,是同一种核素
Pt的核外电子数相同,是同一种核素
B. 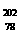 Pt和
Pt和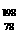 Pt的中子数相同,互称为同位素
Pt的中子数相同,互称为同位素
C. 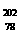 Pt和
Pt和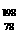 Pt的质子数相同,互称为同位素
Pt的质子数相同,互称为同位素
D. 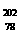 Pt和
Pt和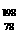 Pt的质量数不同,不能互称为同位素
Pt的质量数不同,不能互称为同位素
1.请你运用所学的化学知识判断,下列有关的叙述错误的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D. 几千万年前地球上一条恐龙体内的某个原子可能在你的身体里
23、实验室用二氧化锰和浓盐酸反应制取氯气。
(1)若用200mL10mol·L-1的浓盐酸与足量的二氧化锰固体加热反应(不考虑氯化氢挥发),则产生氯气的物质的量为 0.50 mol(填“大于”、“等于”或“小于”),原因是 。
(2)870g二氧化锰与足量的浓盐酸反应(二氧化锰的相对原子质量为87g/mol),则被氧化的氯化氢的物质的量是多少?
附加题:(10分,此题只要求实验班、重点班的同学做)
.某同学发现,纯度、质量、表面积都相同的两铝片与c(H+)相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝与盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
⑴.该同学认为:由于预先控制了反应的其它条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因①:Cl-对反应具有促进作用,而SO2- 4对反应没有影响;
原因②: ;
原因③:Cl-对反应具有促进作用,而SO2- 4对反应具有阻碍作用;
原因④:Cl-、SO2- 4均对反应具有促进作用,但Cl-影响更大;
原因⑤: ;
⑵该同学设计并进行了两组实验,即得出了正确的结论。
他取了两片等质量、外形和组成相同、表面积经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的盐酸和稀硫酸的试管中(两试管的规格完全相同)。
① 在盛有稀硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
② 在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化;
或观察到实验①中 ,而实验②中 ,则说明原因③是正确的。依次类推,该同学通过分析实验现象,得出了结论:Cl-对反应具有促进作用。
⑶为了使实验“定量化”、使结果更精确,可以对实验进行比较反应速率:反应时间可以用秒表测定。如果要对上述实验中的反应速率进行比较,可以通过测定哪些物理量来确定?(要求回答一种即可)
。
广东惠阳高级中学2008-2009学年度
22.(14分 )某学生设计如下实验装置用于制备纯净的
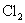 。
。
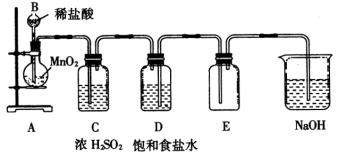
①装置中有多处错误,请指出其中的三处。
(1) ,
(2) ,
(3) ,
②在更正后的装置图中,洗气瓶(净化气体)中的饱和食盐水、浓硫酸、氢氧化钠溶液的作用分别是:
(1)饱和食盐水的作用 ;
(2)浓硫酸的作用 ;
(3)氢氧化钠的作用 。
③该实验中制氯气的原理为(写出制氯气的化学方程式)
21、(7分)书写电子式或用电子式回答下列问题
①NaOH ②H2O ③N2
④以氯化氢为例表示共价键形成 (2分)
⑤以氯化钠为例表示离子键形成 (2分)
20.(9分)在第3周期中,置换酸中氢的能力最强的元素的元素符号为 ,化学性质最稳定的元素符号是 ,最高价氧化物的水化物的酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是 ,显两性的氢氧化物的化学式是 ,该两性氢氧化物与盐酸、氢氧钠溶液分别反应的离子方程式为
、 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com