
题目列表(包括答案和解析)
2.在一定条件下,RO3n-和氟气可发生如下反应:RO3n-+F2+2OH-=RO4-+2F-+H2O。从而可知在RO3n-中,元素R的化合价是
A +4 B +5 C +6 D +7
1.“绿色商品”是指对环境无污染的商品,下列属于“绿色商品”的是
A 含碘食盐 B 含磷洗涤剂 C 含铅汽油 D 含氟冰箱
21、利用铜棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当铜棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。请回答下列问题:
(1)该原电池的正极反应式为:
(2)计算原稀硫酸的物质的量浓度。
(3)若将铜棒换成铁片,仍按题给方式组合起来,能否组成原电池呢? (填“能”或“不能”) 若能组成原电池,此原电池的负极反应式是
。
20、(14分)W、X、Y和Z都是周期表中前18号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为W2Y离子化合物;
②Y和Z属同族元素,它们能形成两种常见的化合物;
③X和Y属同一周期元素,它们能形成组成为XY2共价化合物,一个XY2分子中的电子总数为22;
(1)W元素是 ;Z元素是 。
(2)化合物W2Y和XY2的电子式分别是 和 。
(3)Y和Z形成的两种常见的化合物的分子式是 和 。
(4)写出化合物XY2与W的高价氧化物对应水化物反应的离子方程式:
19、(4分)在下图的装置中,属于原电池的是( )
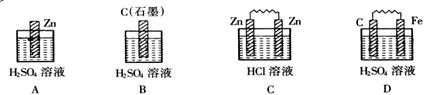
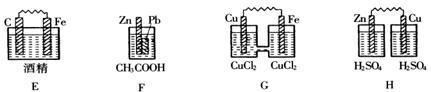
18、(6分) 用化学符号表示符合下列条件的微粒:
(1)含有10个电子的分子有: Ne、 HF 、 、 和 CH4。
(2)含有10个电子的阳离子有: Na+、 、 、 NH4+和 H3O+。
(3)含有10个电子的常见阴离子有: 、 、和 OH-。
16、A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )
A. A、B、C、D、E B. E、C、D、B、A
C. C、D、A、B、E D. B、A、D、C、E


周期
(涉及到填写的物质写元素符号或化学式)
(1) 在这些元素中,化学性质最不活泼的是: ,原子结构示意图为_______ 。
(2) 最高价含氧酸酸性最强的酸是________,碱性最强的化合物是 。
(3) 化合物显两性的氢氧化物是___ ___;写出它的与氢氧化钠反应的离子方程式 。
(4) 用电子式表示元素④与⑦的化合物的形成过程: ,
该化合物属于 (填“共价”或“离子”)化合物。
(5)写出①与⑦形成化合物的分子式 ,该化合物是由 (填“极性”“非极性”)键形成的。
15、同一主族的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性强弱是
H3XO4<H3YO4<H3ZO4,下列推断正确的是( )
A、气态氢化物稳定性:XH3<YH3<ZH3
B、原子序数:X<Y<Z
C、元素的非金属性强弱:X>Y>Z
D、电子层数:Y>X>Z
14、A、B两元素的阴离子具有相同的电子层结构,A元素的阴离子半径大于B元素的阴离子半径,C和A两元素的原子核外电子层数相同,C元素的原子半径大于A元素的原子半径,则A、B、C三种元素的原子序数的关系是( )
A、A>B>C B、B>A>C C、C>A>B D、A>C>B
13、下列电子式书写正确的是( )

 A、 B、
A、 B、

 C、 D、
C、 D、
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com