
题目列表(包括答案和解析)
27、(10分)为探究CO2与过量的NaOH溶液确实发生了化学反应,甲、乙、丙三位同学设计了下列三种实验装置,请回答下列问题:
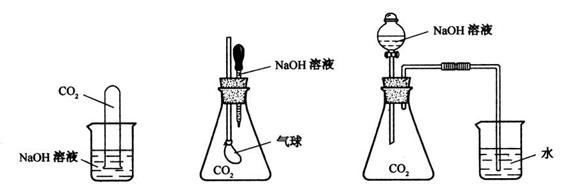 (甲)
(乙)
(丙)
(甲)
(乙)
(丙)
(1)请写出CO2与过量的NaOH发生反应的化学方程式: 。
(2)选择任意一种实验装置,简述预计出现的实验现象,解释产生该实验现象的原因。你选择的实验装置是 ,实验现象是 。 解释产生该实验现象的原因 。
(3)甲、乙、丙同学设计的三个方案中,有一个方案在实际操作中可行性和安全性存在问题,该方案是 。(填甲、乙或丙)
(4)请设计一个实验检验生成的产物中含有Na2CO3。(简述所用试剂、实验现象和结论。)
26.(12分)化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,化学实验室产生的废液必须经处理后才能排放。某化学实验室产生的废液中含有Fe3+、Cu2+、Ag+三种金属离子,实验室设计了下列方案对废液进行处理:

(1)废液经操作①得到的沉淀中含有的金属单质是 ;
写出操作①的反应离子方程式 ; ; 。
(2)在操作②中观察到的实验现象是
(3)操作③中发生主要反应的离子方程式为
25、(12分)氯碱工业中,通过电解饱和食盐水获得重要的化工原料:氯气、氢气和氢氧化钠。其中氯气用途十分广泛,除用于净水、环境消毒外,还用于生产盐酸、硅、聚氯乙烯、氯苯等。
(1)写出氯碱工业中通过电解饱和食盐水获得重要的化工原料氯气的离子方程式
(2)工业上可用氯气和石灰乳为原料制造漂白粉,写出该反应的化学方程式 。
(3)工业上生产半导体材料硅的流程如下:

①写出在制备粗硅时反应的化学方程式_____________________________,在该反应的化学方程式上标出电子的转移方向和数目。此反应中焦炭的作用是____________。(填“氧化剂”或“还原剂”) ②粗硅与氯气反应后得到沸点较低的液态四氯化硅中常混有一些高沸点,难挥发性杂质,必须进行分离提纯。其提纯方法为____________。(填序号)
A.蒸馏 B.过滤 C.萃取 D.结晶 ③由四氯化硅通入氢气得到高纯硅和氯化氢气体,写出该反应的化学方程式:
________________________________________________________________________。
24.(10分)实验室配制0.5mol·L-1的KCl溶液500mL,有以下仪器:
①烧杯 ②胶头滴管 ③1000mL容量瓶 ④500mL容量瓶 ⑤玻璃棒
⑥托盘天平(带砝码) ⑦酒精灯 ⑧量筒
(1)配制时,称量时必须使用的仪器有 (填代号)
(2)该实验两次用到玻璃棒,其作用分别是 、
(3)配制时一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④转移 ⑤洗涤
⑥定容 ⑦摇匀(要用到两次) ⑧冷却
其正确的操作顺序为②①③ ⑦⑥
(4)试计算应称取的KCl固体的质量为 g。在定容时视线应
23.下列反应中,不能用离子方程式Ba2++SO42-=BaSO4↓来表示的是( )
A.稀硫酸溶液与硝酸钡溶液反应
B.硫酸钾溶液与氯化钡溶液反应
C.稀硫酸溶液与氢氧化钡溶液反应
D.硫酸钠溶液与硝酸钡溶液反应
22.将一定质量的Mg、Zn、Al混合物与足量稀H2SO4反应,生成H2 2.24 L(标准状况),原混合物的质量可能是 ( )
A. 1.8 g B.6.5 g C.3 g D.10 g
21.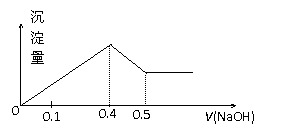 现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为 ( )
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为 ( )
A.1:3 B.2:3
C.6:1 D.3:1
20.科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列关于硅的说法中正确的是 ( )
A.自然界中硅元素的含量最丰富 B.自然界中存在大量单质硅
C.高纯度的硅被用于制作计算机芯片 D.光导纤维的主要成分是Si
19、铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途。下列关于铝的说法不正确的是( )
A. 铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B. 常温下不与任何酸、碱反应
C.铝元素在地壳中的含量高,储量丰富
D.工业上可以用电解法冶炼铝
18、 适量下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是( )
A、碘水 B、溴化钠溶液 C、氯水 D、溴水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com