
题目列表(包括答案和解析)
3、在铁制品上镀一定厚度的锌层,以下方案设计正确的是 ( )
A.锌做阳极,镀件做阴极,溶液中含有锌离子
B.铂做阴极,镀件做阳极,溶液中含有锌离子
C.铁做阳极,镀件做阴极,溶液中含有亚铁离子
D.锌做阴极,镀件做阳极,溶液中含有锌离子
2、可以将反应Zn+Br2==ZnBr2设计成蓄电池,下列四个电极反应
①Br2+2e-=2Br- ②2Br--2e-= Br2 ③Zn-2e-=Zn2+ ④Zn2++2e-=Zn
其中表示充电时的阳极反应和放电时的负极反应的分别是 ( )
A.②③ B.②① C.③① D.④①
1、原电池的正极和电解池的阴极所发生的反应分别是 ( )
A.氧化、还原 B.还原、氧化 C.氧化、氧化 D.还原、还原
2、在25℃时.将两个铂电极插入一定量的饱和Na2SO4溶液中进行电解,通电一段时间后在阴极逸出a摩气体,同时析出w克Na2SO4·10H2O晶体,若温度不变,此时剩余溶液的质量分数是 ( )
A. B.
B.
C. D.
D.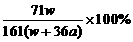
解析:用铂做电极电解饱和Na2SO4溶液,实质上电解水,因水电解时分解成氢气和氧气,因而溶液中有晶体Na2SO4·10H2O析出,析出来的晶体和电解消耗掉的水为原饱和溶液的一部分,由此可确定C 选项符合题意。本题着重考查学生审题能力以及对电解知识的理解和应用。
[随堂检学]
1、在电解水时,常加入一些稀硫酸,其目的是 ( )
A.使溶液酸性增强 B.使溶液中离子浓度增大
C.加快电解的速率 D.使溶液的氧化性增强
解析:纯水导电性很弱,向水中加入一些电解质可增强导电性,如:稀硫酸、氢氧化钠固体等,故选BC。
2、 电极反应式和总反应式的书写
要学会在理解电解原理的基础上,熟练掌握电极反应式和总反应式的书写。
1、阴阳极的判断
电解池的阴极和阳极与电极材料无关,取决于外电源的正负极。与电源正极相连的为电解池的阳极;与电源负极相连的为电解池的阴极。
2、电解原理的应用
(1)铜的电解精炼
电解精炼粗铜时,阳极材料是 铜,
阴极材料是 铜,电解质溶液是 溶液。
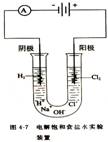 (2)电解饱和食盐水制取氯气和烧碱(氯碱工业)
(2)电解饱和食盐水制取氯气和烧碱(氯碱工业)
电解前应除去食盐溶液中的Ca2+、Mg2+、SO42- 等杂质离子
电极反应:
阳极反应 ,
阴极反应 ,
电解反应为 。
(3)电镀
电镀是一种特殊的电解,要求镀件必须作阴极,阳极、电解质溶液中的阳离子、镀层金属都必须是同一种金属元素。电镀时,电解质溶液的浓度保持不变。
(4)冶炼活泼金属(铝、钠、镁等)
|
如:2Al2O3=== 4Al + 3O2↑
1、电解氯化铜溶液
(1)电极名称
与电源正极相连的电极称为 极;
与电源负极相连的电极称为 极。
(2)电极反应、电解反应
阳极发生的电极反应为 ;
阴极发生的电极反应为 ;
电解反应的化学方程式为 ;
电解反应的离子方程式为 。
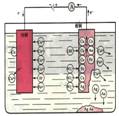 (3)电子流动方向
(3)电子流动方向
从电源负极流出、流向电解槽的阴极,从电解槽的阳极流向电源的正极。
(4)能量转化
反应中 能转化为 能
6.现有X、Y、Z三种物质,各取40g相混合,完全反应后,得Y 18g,Z 49g,还有W生成。已知W的式量为106,现将22gX和11gY反应,能生成W为( )
A、0.5mol B、0.25mol C、53g D、26.5g

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com