
题目列表(包括答案和解析)
2.生命起源的研究是世界性科技领域的一大课题,科学家认为生命起源的第一层次是产生与硝基化合物可能是同分异构体的物质,这类物质是( )。
 A.糖
B.氨基酸 C.醇
D.羧酸
A.糖
B.氨基酸 C.醇
D.羧酸
1.一次性餐具目前最有发展前景的是( )。
A.瓷器餐具 B.淀粉餐具 C.塑料餐具 D.纸木餐具
23.A、B两元素,A的原子序数为x,A和B所在周期的元素种类总数分别是m和n。
(1)如果A和B同在第ⅠA族,当B在A的上一周期时,B的原子序数为 ,当B在A的下一周期时,B的原子序数为 。
(2)如果A和B同在第ⅦA族,当B在A的上一周期时,B的原子序数为 ,当B在A的下一周期时,B的原子序数为 。
资料卡片
元素周期表发展的远景
元素周期表中的元素已经编排到112号,元素周期表还能不能延长?根据现有的理论计算第7周期应有32种元素,至118号元素结束。
第8周期应有50种元素,至168号。同理,第9周期也应有50种元素,至218号。
有趣的是,有些科学家还提出元素周期表还可以向负方向发展,这是由于发现了正电子、负质子(反质子)。在其他星球上是否存在由这些反质子和正电子以及中子组成的反原子呢?这种观点若能被实践证实,周期表当然可以出现原子核带负电荷的反元素,向负方向发展也就顺理成章了。
轻松一题: 试写出由负质子、正电子构成的反氢离子、反氢氧根离子的中和反应方程式。 答案: H-+OH+ ==H2O
自我反馈
导学园地

22.制冷剂是易被压缩、液化的气体,液化后在管内循环,蒸发时吸收热量,使环境温度降低,达到制冷目的。人们曾采用过乙醚、NH3、CH3Cl等作制冷剂,但它们不是有毒,就是易燃。于是科学家根据元素性质的递变规律来开发新的制冷剂。
据现有知识,某些元素化合物的易燃性、毒性变化趋势如下:
(1)氢化物的易燃性:第二周期 > >H2O>HF;第三周期SiH4>PH3>H2S>HCl。
(2)化合物的毒性:PH3>NH3;H2S H2O; CS2 CO2;CCl4>CF4(选填“>”“<”或“=”)。
于是科学家们开始把注意力集中在含F、Cl的化合物上。
(3)已知CCl4的沸点为76.8 ℃,CF4的沸点为?-128 ℃?,新的制冷剂的沸点范围应介于其间。经过较长时间反复试验,一种新的制冷剂氟利昂CF2Cl2终于诞生了,其他类似的还可以是 。
(4)然而,这种制冷剂造成了当今的某一环境问题,是 ,但求助于周期表中元素及其化合物的 变化趋势来开发制冷剂的科学思维方法是值得借鉴的(填写字母)。
①毒性 ②沸点 ③易燃性 ④水溶性 ⑤颜色
a.①②③ b.②④⑤ c.②③④
21.A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: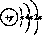 ,B、C可形成离子化合物B3C2,据此填空:
,B、C可形成离子化合物B3C2,据此填空:
(1)A的元素名称为 ,其气态氢化物的化学式为 。
(2)A、B、C、D四种元素的原子,半径由小到大的顺序为 。
(3)B和C最高价氧化物的水化物化学式分别为 和 。
20.现有A、B、C、D四种短周期元素,已知A、B同主族,B、C、D同周期,A、B的原子序数之和等于C、D的原子序数之和,C的最高价氧化物的水化物能分别跟B和D的最高价氧化物的水化物反应。请回答:
(1)B和C的元素符号分别为B ,C 。
(2)上述四种元素的原子半径由大到小的顺序(用元素符号表示)为 。
(3)D单质在A单质中燃烧的产物与二氧化碳反应的化学方程式为 。
(4)写出B元素在周期表中的位置 。
(5)写出C的最高价氧化物的水化物分别跟B和D的最高价氧化物的水化物反应的方程式 。
19.A、B、C为短周期元素,在周期表中所处位置如图所示。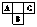
A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。
(1)写出A、B、C三种元素的名称: 、 、 。
(2)B位于元素周期表第 周期,第 族。
(3)C的原子结构示意图为 。
(4)比较B、C的原子半径:B C,写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式 。
18.若ⅡA族某元素原子序数为x,那么原子序数为x +1的元素可能位于( )
A.ⅢA族 B.ⅠB族
C.ⅡB族 D.Ⅷ族
17.已知a为ⅡA族元素,b为ⅢA族元素,它们的原子序数分别为m和n,且a、b为同一周期元素,下列关系错误的是( )
A. n = m +1 B. n = m+11
C. n = m +25 D. n=m+10
16.下列关于微粒半径的说法正确的是( )
A.电子层数少的元素的原子半径一定小于电子层数多的元素的原子半径
B.核外电子层结构相同的单核微粒半径相同
C.质子数相同的不同单核微粒,电子数越多半径越大
D.原子序数越大,原子半径越大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com