
题目列表(包括答案和解析)
0.01mol / L FeCl3和 0.01mol / LKSCN等体积混合
 ①加1mol / L FeCl3 红色加深
①加1mol / L FeCl3 红色加深
②加1mol / L KSCN 红色加深
1、 浓度对Fe3+(棕黄)
+ 3SCN- (无色) Fe(SCN)3(血红色)反应平衡状态的影响:
浓度对Fe3+(棕黄)
+ 3SCN- (无色) Fe(SCN)3(血红色)反应平衡状态的影响:
2.化学平衡
(1)化学平衡状态是:
。
[质疑]化学平衡的特征是什么?为什么说化学平衡是动态平衡?
(2)化学平衡的特征
动:
定:
变:
[质疑]化学平衡随条件的变化而变化,哪些条件对化学平衡有影响?
[观察·思考]温度对NO2与N2O4反应平衡状态是如何影响的?为什么条件的改变平衡状态被破坏?
 [阐述]在2NO2(红棕色) N2O4(无色)的反应中(已知生成N2O4的反应是放热反应);
[阐述]在2NO2(红棕色) N2O4(无色)的反应中(已知生成N2O4的反应是放热反应);
浸入冷水中气体颜色变浅,说明NO2的浓度 ,这是因为
浸入热水中气体颜色 ,说明NO2的浓度 ,这是因为升高温度有利于NO2的生成。
温度的改变使正、逆反应速率不等,原平衡被破坏,可见化学平衡是在一定条件下建立的,同一可逆反应条件不同平衡状态不同,即化学平衡发生移动。
(3)化学平衡移动:化学平衡只有在一定的条件下才能保持平衡。如果一个可逆反应达到平衡状态以后, 改变了,平衡混合物里各组成物的质量分数也就随之改变而达到新的平衡状态,这叫化学平衡的移动。

[知识拓展]
[实验探究]补充浓度、压强对化学平衡移动的影响
1.可逆反应:
[注意]同一条件,同时进行;反应物不能完全转化为生成物。
[质疑]氢气和氧气在一定条件下能反应生成水,水在一定条件下又能分解为氢气和氧气,水的分解反应是可逆反应吗?还有哪些反应是可逆反应?
[质疑、讨论]常温下,在100g水中加入100g氯化钠固体,能否溶解完全(氯化钠的溶解度小于100g)?在一定温度下的氯化钠的饱和溶液中加入氯化钠固体能否溶解?

[质疑、探讨]一定条件下的可逆反应能否出现正、逆反应速率相等?
 请在下图中画出反应A(g) +
B(g) C(g) + D(g)的反应速率和反应时间的关系图。
请在下图中画出反应A(g) +
B(g) C(g) + D(g)的反应速率和反应时间的关系图。


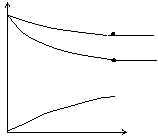
11.某温度时,在2升容器中X、Y、Z三种物质的物质的量随时间的变化曲线如右图所示。由图中数据分析,该反应的化学方程式为 ;反应开始至2分钟的平均反应速率为_________________。
[布置作业]:
[课题] 二、化学反应的限度
[第2课时]
[质疑]在学习二氧化硫的性质时有两个重要的反应,体现二氧化硫的还原性和氧化性:

 2SO2
+ O2 2SO3
, SO2 + 2H2S = 3S + 2H2O 。为什么一个式子用“
”,一个式子
2SO2
+ O2 2SO3
, SO2 + 2H2S = 3S + 2H2O 。为什么一个式子用“
”,一个式子
用“=”号?说明什么?
10.已知反应A+3B=2C+D,在某段时间内以A的浓度变化表示的速率为1mol/(L·min),则此段时间内以C的浓度变化表示的化学反应速率:
 物质的量(mol) 物质的量(mol)1.0- 0.9   0.8-
Y
0.6- 0.7 X 0.4-
0.2- 0.2 Z 0.8-
Y
0.6- 0.7 X 0.4-
0.2- 0.2 Z      1 2 3 4 5
1 2 3 4 5时间(分) |
9.某温度时,把1mol气体A2(单质)和1mol气体B2(单质)放入容积为1L的密闭容器中,使其反应生成气体C,2min后,测得容器中C(A2)==0.4mol/L,C(B2)==0.8mol/L,C(C)==0.4mol/L.则此反应的化学方程式为:__________________________________________.
8. 用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A.加热 B.不用稀硫酸,改用98%浓硫酸
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
7. 反应2SO2+O2 2SO2经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为
反应2SO2+O2 2SO2经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为
A.0.1s B.2.5s C.5s D.10s
6. 在恒温恒容条件下,能使A(g)+B(g) C(g)+D(g)正反应速率增大的措施是
在恒温恒容条件下,能使A(g)+B(g) C(g)+D(g)正反应速率增大的措施是
A.减小C或D的浓度 B.增大D的浓度 C.减小B的浓度 D.增大A或B的浓度
[B 组]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com