
题目列表(包括答案和解析)
4.化学反应的实质:旧化学键的断裂和新的化学键的形成的过程。
 三、典型例题:
三、典型例题:
例1:下列说法正确的是: ( )
A.含有离子键的化合物必是离子化合物
B.含有共价键的物质就是共价化合物
C.共价化合物可能含有离子键
 D.离子化合物中可能含有共价键
D.离子化合物中可能含有共价键
解析:只要含有离子键,其构成物质的微粒必为阴阳离子,必定形成离子化合物。但共价键除共价化合物含有外,某些单质中、某些离子化合物的复杂离子中也含有共价键。
答案:AD。
例2:下列电子式书写正确的是 ( )
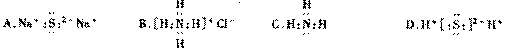
答案:C。
例3:已知氯化铝的熔点为190℃(2.02×105Pa),但它在180℃即开始升华。
(1)氯化铝是_____________(填“离子化合物”或“共价化合物”)。
(2)在500K和1.01×105Pa时,它的蒸气密度(换算成标准状况时)为11.92g·L-1,且已知它的结构中有配位键,氯化铝的化学式为_____________,结构式为________________。(在共价键中,如果电子对是由一个原子A单方面提供而跟另一个原子B共用的共价键叫配位键。配位键表示为“A→B”的形式。)
(3)设计一个可靠的实验,判别氯化铝是离子化合物还是共价化合物。你设计的实验是_______
_______________________________________________________。


 解析:(1)离子化合物熔沸点较高,从氯化铝的性质,熔点低,易升华等,可推测,氯化铝应属于共价化合物。 Cl Cl Cl
解析:(1)离子化合物熔沸点较高,从氯化铝的性质,熔点低,易升华等,可推测,氯化铝应属于共价化合物。 Cl Cl Cl



 (2)Al2Cl6 Al Al
(2)Al2Cl6 Al Al
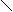 Cl
Cl Cl
Cl
Cl Cl
(3)在其熔融状态下,试验其是否导电,若不导电则证明氯化铝是共价化合物。
[随堂检学]
3.

 结构式:将共价分子中,每一对共用电子对都用一条短线表示,从而表示共价分子中各原子的连接方式的式子。例:N N ,H-Cl,O C O 等。在有机化合物中,可省略结构式中所有的碳氢键和碳碳单键,写成结构简式。
结构式:将共价分子中,每一对共用电子对都用一条短线表示,从而表示共价分子中各原子的连接方式的式子。例:N N ,H-Cl,O C O 等。在有机化合物中,可省略结构式中所有的碳氢键和碳碳单键,写成结构简式。
2. ①单质分子的形成:如:H2、Cl2、N2等。
①单质分子的形成:如:H2、Cl2、N2等。
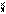


 H + H
H H
H + H
H H
两个不稳定的氢原子 稳定的氢分子 (共价分子)

 放出能量
放出能量
能量较高 能量较低
吸收能量
②共价化合物的形成:如:HCl、H2S、NH3、CCl4等






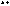




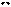

 H
+ S + H
H S H
H
+ S + H
H S H
共价化合物:相邻原子间以共价键结合,这样的化合物,称共价化合物。共价化合物中,只含有共价键,不含有离子键。但离子化合物中可含有共价键,如铵盐(NH4Cl)等。
△共价键:原子间通过共用电子对所形成的强烈的相互作用,称共价键。共价键可存在于 单质、共价化合物、离子化合物中。
1.非金属元素的原子之间成键时,要成为稳定结构,不能通过得失电子形成阴阳离子,则可通过形成共用电子对等方式。
4.学会用结构简式表示有机化合物分子。学会运用结构模型、化学用语进行化学的研究和学习。
3.知道不同的共价键的键能是不同的,了解键能大小与键的牢固程度的关系。
2.学会用电子式、结构式表示共价键及共价分子,了解共价化合物的概念。
1.掌握共价键的概念,了解共价键的形成规律。
18.(6分)理论上1g葡萄糖在体内完全氧化成CO2气体和液态水(有氧氧化)释
放出16kJ的能量。在体内这一氧化过程释放的能量由ATP截获被人利用;C6H12O6+6O2+38H3PO4+38ADP →6CO2+44H2O+38ATP
ATP +H2O→ADP +H3PO4 △H =-30.6kJ/mol
(1).写出葡萄糖完全氧化为CO2气体和液态水的热化学方程式
(2).葡萄糖在体内完全氧化为CO2气体和液态水,能量的利用率是多少?
17. 分)由碳棒、铁片和200mL稀H2SO4组成的原电池中,当在碳棒上共放出3.36L(标准状况)气体时,求消耗铁多少克?有多少个电子通过了电线?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com