
题目列表(包括答案和解析)
2.C60与现代足球 有很相似的结构,它与石墨互为
( )
有很相似的结构,它与石墨互为
( )
A.同位素 B.同素异形体 C.同分异构体 D.同系物
1. 下列反应既是氧化还原反应,又是放热反应的是
( )
下列反应既是氧化还原反应,又是放热反应的是
( )
A.铝与稀盐酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与二氧化碳的反应
D.甲烷在氧气中的燃烧反应
23. 铅蓄电池是化学电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O根据上述情况判断
⑴蓄电池的负极是_________,其电极反应式为
⑵蓄电池的正极是_________,其电极反应式为
⑶蓄电池工作时,其中电解质溶液的PH_______(增大、减小、不变)
(4)若用该蓄电池作电源(都用惰性材料做电极)电解400g饱和食盐水,如果电池内
硫酸的的体积为5升,当其浓度从1.5mol/L降至1.3mol/L时,计算剩余溶液中氯化钠的质量分数。(该温度下氯化钠的溶解度为32克)
22. (9分)现有碳酸氢钠、碳酸钠晶体(Na2CO3·xH2O)的混合物,为了测定x值,某同学采用如下图所示装置进行实验,回答下列问题:
⑴ A装置的作用是
⑵ B装置的作用是
⑶ C装置的作用是 。
⑷你认为该装置有什么不足


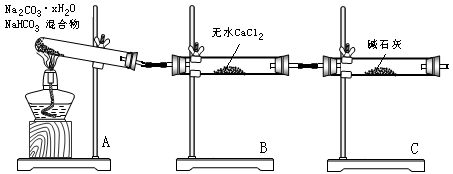
(5)若在试管A中装有碳酸氢钠和Na2CO3·xH2O混合物33.4g,用酒精灯加热到反应完全,此时B管增加质量15.3g,C管增加质量2.2g,则x的值为 。
21. 经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。
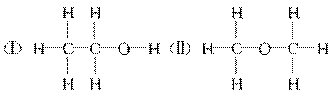
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁四位同学直接利用如图给定装置开始进行实验确定乙醇的结构。
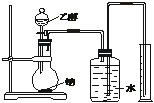
(1)学生甲得到一组实验数据:
|
乙醇的物质的量/mol |
氢气的体积/L |
|
0.10 |
1.12(标准状况) |
根据以上数据推断乙醇的结构为 (用Ⅰ、Ⅱ表示),理由为
(2)同学乙分别准确称量4.60 g 乙醇进行多次实验,结果发现以排开量筒内的体积作为生成的H2体积,换算成标准状况后都小于1.12L,如果忽略量筒本身及乙同学读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗? (填“正确”或“不正确”)。如果你认为正确,请说明理由;如果你认为不正确,那产生这种情况的原因应该是什么?
(3)同学丙认为实验成功的关键有:①装置气密性要良好,②实验开始前准确确定乙醇的量,③钠足量,④广口瓶内水必须充满,⑤氢气体积的测算方法正确、数据准确。其中正确的有 。(填序号)
(4)同学丁不想通过称量乙醇的质量来确定乙醇的量,那么他还需要知道的数据是 。
(5)实验后,四名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是 。
19.(1)、分析下列物质的物理性质,判断其晶体类型:
A.碳化铝,黄色晶体,熔点2200OC,熔融态不导电________________________;
B.溴化铝,无色晶体,熔点98OC,熔融态不导电__________________________;
C. 五氟化钒,无色晶体,熔点19.5OC,易溶于乙醇、氯仿、丙酮中____________;
D.溴化钾,无色晶体,熔融时或溶于水中都能导电_________________________。
(2)具有双核10个电子的共价化合物的化学式是 ,三核10个电子的共价化合物的化学式是 ,四核10个电子的共价化合物的化学式是 ,五核10个电子的共价化合物的化学式是
(3)患有糖尿病的人的尿中含有葡萄糖,设想怎样去检验一个病人是否患有糖尿病?
(4)A元素的氯化物的化学式为ACly,分子中各原子最外层电子数之和为26,
则y的值为
(5)原电池、电解池在工作时,各极的质量变化有以下三种可能:
①变大 ②变小 ③不变(写出一种最常见的变化) (1)负极质量变化可能是 (2)正极质量变化可能是
(3)阴极质量变化可能是 (4)阳极质量变化可能是 20.右图是等质量的Na2CO3、NaHCO3粉末分别与足量的
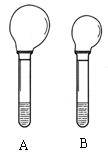 盐酸发生反应时的情景,产生CO2气体的体积较多的试
盐酸发生反应时的情景,产生CO2气体的体积较多的试
管中加入的固体试剂是________,当反应结束时,A、B
两试管中消耗的盐酸的质量之比为__________。
 实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管中的此反应过程中,反应体系的能量变化的总趋势分别对应于A-____,B-____。(填写a或b)
实验过程中我们还能感受到Na2CO3与盐酸反应时是放热反应,而NaHCO3与盐酸反应时表现为吸热。在A、B两试管中的此反应过程中,反应体系的能量变化的总趋势分别对应于A-____,B-____。(填写a或b)
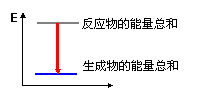


(a) (b)
18.已知在25℃,101kPa下,lgC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是 ( )
A.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(g);△H=-48.40kJ·mol-1
B.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1);△H=-5518kJ·mol-1
C.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1);△H=+5518kJ·mol-1
D.C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1);△H=-48.40kJ·mol
第Ⅱ卷(非选择题,共46分)
16.当干冰气化时,下列所述中发生变化的是 ( )
A.分子间距离 B.、范德华力 C.分子内共价键 D.化学性质
|
|
|
|
|
15.下列性质中,可证明某化合物内一定存在离子键的是 ( )
A.可溶于水 B.具有较高的熔点 C.水溶液能导电 D.熔融状态能导电
14.下列说法中正确的是 ( )
 A.周期表是按原子量逐渐增大的顺序从左到右排列的
A.周期表是按原子量逐渐增大的顺序从左到右排列的
B.最外层电子数相同的元素都是同一族
C.同主族元素的最外层电子数一定相同
D.同周期元素的电子层数相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com