
题目列表(包括答案和解析)
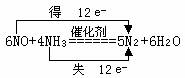
13、⑴
⑵0.3、0.7或0.8、0.2
12、⑴小烧杯(或表面皿) ⑵500mL容量瓶 ⑶定容
⑷偏低 偏低 无影响 偏高
⑸①药匙 托盘天平 烧杯 玻璃棒 胶头滴管
 ②容量瓶
②容量瓶
1-5 BDDBA 6-11 CCACDC
13. 已知在加入催化剂的条件下NO和NH3可以反应生成N2和H2O。现在有NO和NH3的混合物1mol,充分反应后还原产物得到的N2比氧化产物得到的N2多1.4g.
⑴写出反应的化学方程式,并标明电子转移的方向和数目;
⑵若以上反应完全进行,试计算混合物中NO和NH3的物质的量各是多少?
参观答案:
12. 实验室配制500 mL 0.1mol/L的氢氧化钠溶液,请回答下列问题:
⑴称量氢氧化钠固体时应放在 中进行:
 ⑵配制时应选用 容量瓶;
⑵配制时应选用 容量瓶;
 ⑶在此配制过程中胶头滴管的作用是 ;
⑶在此配制过程中胶头滴管的作用是 ;
 ⑷若实验时遇到下列情况,将会使所配的溶液浓度发生什么变化(填“偏高”“偏低”或“无影响”):
⑷若实验时遇到下列情况,将会使所配的溶液浓度发生什么变化(填“偏高”“偏低”或“无影响”):
A.加水定容时超过刻度线 ;
 B.没有将洗涤液转入容量瓶中 ;
B.没有将洗涤液转入容量瓶中 ;
 C.容量瓶内壁沾有水滴没有烘干就进行配制 ;
C.容量瓶内壁沾有水滴没有烘干就进行配制 ;
 D.定容时俯视
;
D.定容时俯视
;
 ⑸与配制5%的氢氧化钠溶液相比:
⑸与配制5%的氢氧化钠溶液相比:
①用到的相同仪器: ;
 ②用到的不同仪器:
;
②用到的不同仪器:
;
11. 已知有下列反应,从化合价角度分析哪一个表示二氧化硫被还原
A.SO2+2H2O+CL2===H2SO4+2HCL B.SO2+2NaOH===Na2SO3+H2O
 C.SO2+2H2S===2H2O+3S
D.SO2+PbO2===PbSO4
C.SO2+2H2S===2H2O+3S
D.SO2+PbO2===PbSO4
10. 配制100mL 0.1mol/L Na2CO3溶液,下列操作正确的是
A.称取10.6g无水碳酸钠,加入100mL 的容量瓶中,加水溶解.定容
B.称取10.6g无水碳酸钠,加入100mL 蒸馏水,搅拌.溶解
C.转移Na2CO3溶液时,直接倒入容量瓶中
D.定容后塞好瓶塞,反复倒转.摇匀后倒入试剂瓶中
9. 一个体积不变的密闭容器中盛有11gCO2时,压强为1×104Pa。如果在相同温度下,把更多的CO2充入容器中,使容器内压强增至5×104Pa,这时容器内气体的分子数约为
A.3.3×1025 B.3.3×1024 C.7.5×1023 D.7.5×1022
8. 下列条件下,两瓶气体所含有的原子数一定相等的是
A.相同质量.不同密度的N2和CO B.同温度.同体积的H2和N2
C.同体积.同密度的CH4和NH3 D.同压强.同体积的SO2和CO2
7. 下列叙述中,正确的是
A.氯化钠溶液在电流作用下电离成Na+和CL-
B.溶于水后能电离出H+的化合物都是酸
C.BaSO4难溶于水,但BaSO4属于电解质
D.CO2溶于水能部分电离,故CO2属于电解质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com