
题目列表(包括答案和解析)
1.分类法与比较法
[自主研学] :
在研究物质的性质时,运用 的方法,分门别类的对物质及其变化进行研究,可以总结出各类物质间的 和 ;运用 的方法,可以找出物质间的异同,认识物质性质间的 。
[互动探究]:
(1).运用所学知识,比较金属钠与金属铁的性质。
|
物质 |
钠 |
铁 |
||
|
物理性质 |
相同点 |
|
||
|
不同点 |
|
|
||
|
化学性质 |
相同点 |
|
||
|
不同点 |
|
|
||
(2).根据所学的知识和已有的生活经验,预测金属可能具有哪些共同的性质?
(3).在研究金属钠的性质的过程中,你运用了哪些研究方法?
2. 实验法:是验证
或
的过程。
实验法:是验证
或
的过程。
(1).实验的要求:
实验前, ;
实验中, ;
实验后, 。
(2).实验进行时,要注意控制 、 、 等条件,这是因为 。
(3).实验探究:金属钠与氧气的反应
[实验目的]:①.探究金属钠与氧气反应;
②.认识条件控制在实验研究中的意义。
[实验仪器和试剂]:金属钠、酒精灯、石棉网、铁架台、铁圈
[实验步骤]:①.将切好的金属钠放置在空气中,使其与氧气反应。
②.将金属钠放在石棉网上加热,使其与氧气反应。

 [实验现象与记录]:①.钠在空气中放置,表面很快变
、生成一种 色固体
。
[实验现象与记录]:①.钠在空气中放置,表面很快变
、生成一种 色固体
。
②.在空气中加热,先熔化成闪亮的小球,然后剧烈反应,发出 火焰,生成一种 色固体 。
[实验结论]:钠很容易被氧化,在常温下能跟空气中氧气化合而生成没有金属光泽的Na2O,
反应的化学方程式: ;而钠在受热时,剧烈反应生成淡黄色的Na2O2固体,反应的化学方程式: 。
特别提示:
(1).许多化学反应若使反应物按不同的量比或采用不同的条件,则可能得到不同的产物。如:钠与氧气的发应,常温下生成氧化钠、受热时生成过氧化钠;炭与氧气的反应,
在足量的氧气中燃烧生成CO2,不足量的氧气中燃烧时生成CO。除此以外,在今后的学习中还要学到许多这样的反应,以后的学习中要注意归纳总结。
(2).Na2O和Na2O2的比较
|
氧化物 |
Na2O |
Na2O2 |
|
氧元素的化合价 |
―2 |
―1 |
|
类别 |
碱性氧化物 |
过氧化物 |
|
生成条件 |
常温 |
加热 |
|
颜色、状态 |
白色固体 |
淡黄色粉末 |
(续表)
|
氧化物 |
Na2O |
Na2O2 |
|
与H2O的反应 |
Na2O+H2O=2 NaOH |
2Na2O2+2H2O=4
NaOH+O2↑ |
|
与CO2的反应 |
Na2O+ CO2= Na2CO3 |
2Na2O2+2CO2=2Na2CO3+O2↑ |
|
与酸的反应 |
 Na2O+2HCl=2NaCl+ H2O Na2O+2HCl=2NaCl+ H2O |
2Na2O2+4
HCl=4NaCl+2H2O+O2↑ |
|
热稳定性 |
不稳定,易被氧化成Na2O2 |
较稳定 |
|
漂白作用 |
无 |
有 |
|
用途 |
-- |
强氧化剂、漂白剂、供养剂 |
[互动探究]:
(1).钠放置在空气中会经过怎样的一系列变化?最后生成什么产物?
(2).实验室中由钠着火了,能用水或泡沫灭火器灭火吗?
[质疑激趣]:研究钠及其化合物的性质时,除运用了观察法、实验法,还运用了分类与比较的方法,它们具体有是怎样?
[质疑激趣]: 依据化学科学的含义可知:认识物质的性质是化学研究的一种重要任务。则怎样才能更科学的认识物质的性质呢?
[自主研学] :
研究物质的性质,常常运用 、 、 、
等方法。
1.

 观察法:是一种
观察法:是一种
的方法。
(1).要求:观察时,要有 的目的,要对观察到的现象进行
和 。
(2).[观察探究]:金属钠的物理性质及钠与水反应的现象
[观察目的]:①.认识金属钠的状态、颜色、硬度和密度的相对大小、熔点的相对高低。
②.认识金属钠与水的反应。
[观察内容]:①.观察盛放在试剂瓶中的金属钠。用镊子将金属钠从试剂瓶中取出,用滤纸将其表面的煤油吸干(注意:钠存放在煤油中),在玻璃片上用小刀切下一小块钠(黄豆粒大小),观察钠块的切面。(注意:金属钠有强烈的腐蚀性,千万不要用手直接接触它)其余的钠要迅速放回原瓶中。(注意:一般取用后剩余的试剂不能放回原瓶)
②.向培养皿中加适量的水,滴入1―2滴酚酞溶液,将切好的钠投入到水中,观察现象。
 [观察结论]:①.金属钠的物理性质:色有金属光泽的固体,质软(比铁软),密度小(比水小、比煤油大),熔点(高或低)。
[观察结论]:①.金属钠的物理性质:色有金属光泽的固体,质软(比铁软),密度小(比水小、比煤油大),熔点(高或低)。
②.金属钠与水的反应现象:
Ⅰ.钠浮在水面上,说明 。
Ⅱ.钠块熔成闪亮的小球,说明 。
Ⅲ.钠球迅速向各个方向游动,说明 。
验证得知:气体为 。
Ⅳ.听到液面上发出嘶嘶的响声,说明 。
Ⅴ.滴有酚酞的溶液变红色,说明 。
 因此:钠与水反应的化学方程式:
。
因此:钠与水反应的化学方程式:
。
[互动探究]:
(1).金属钠是怎样保存的?为什么?
(2).金属钠能置换出硫酸铜溶液中的铜吗?
[质疑激趣]:在研究钠的性质过程中,通过观察钠的外观(颜色、状态),借助仪器(小刀切割)测其硬度以及做钠与水的实验等,这实质上也运用了实验的方法,对物质性质进行预测和探究,则实验法对物质的性质是怎样预测和探究的?
8.下图中各量之间可相互计算,试填写求算时的计算方法
物质的质量m
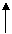




 微观粒子数N 物质的量n
气体的体积V
微观粒子数N 物质的量n
气体的体积V
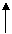
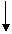
物质的量浓渡CB
 (注:每步计算都可反向进行,请思考计算方法)
(注:每步计算都可反向进行,请思考计算方法)

7.误差分析:下列情况会造成所配制的溶液浓度发生怎样变化 (填偏低、偏高或不变)
(1)容量瓶使用前经蒸馏水清洗后没有干燥 (2)配制过程中,未用蒸馏水洗涤烧杯和玻璃棒 (3)定容时俯视 定容时仰视 (4)用敞口容器称量NaOH且时间过长 (5) 不洗涤烧杯、玻璃棒 (6) 在烧杯中溶解固体或稀释浓溶液时,不放置至室温,而趁热转入容量瓶进行定容 (7)定容后上下倒置摇匀,发现液面低于刻度线时,再加水至刻度线 (8) 定容时加水超出刻度线,又用滴管把多余的溶液取去 (9) 在溶解、转移和洗涤过程中,把溶液溅到容器外
6. 配制一定物质的量浓度的溶液时,为了浓度准确,你认为下列配制步骤中,应该注意什么?称量 ,溶解 ,移液 ,定容 。
5.配制一定物质的量浓度的溶液通常要有以下几个步骤 、 、 、 、 。
4.容量瓶是用于配制 体积 浓度的溶液的容器,在使用之前必须先 。其瓶颈上有一道 ,瓶壁上标有 和 ,此三者的含意是 。所以,在配制溶液过程中,热或冷的溶液一定要 后才能转移到容量瓶中。
3.要通过溶液中的反应定量测定某待测溶液中溶质的含量,往往需要首先配制标准溶液,再将标准溶液与 反应,最后通过对 的处理来确定其溶质的含量。
2.若某溶液的体积为V,其中所含溶质的物质的量为n ,则溶质B的物质的量浓度c(B) = 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com