
题目列表(包括答案和解析)
1.核外电子运动特征:(1)核外电子的特征:⑴电子的质量极___(____kg);
⑵电子绕核运动是在_______的空间(原子的直径约___m)中进行;⑶电子绕核作__速运动(运动的速度接近__,约为__)。
(3)核外电子运动特征:电子绕核运动__确定的轨道,__精确测定或计算电子在任一时刻所在的位置,____描绘出其运动轨迹。我们只能指出___________。
(3)电子层与离核远近及能量高低关系:
|
层序数 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
电子层符号 |
K |
L |
M |
N |
O |
P |
Q |
|
离核远近 |
|
||||||
|
能量 |
|
24.某核素ZAX的氯化物XCl21.11g配成溶液后,需用1mol/L的硝酸银溶液20mL才能把氯离子完全沉淀下来,试计算:
(1)X的质量数。
(2)若X的核内中子数为20,求37gXCl2中所含质子的物质的量是多少?
23.(10分)A、B、C是短周期里的3种元素的单质,甲、乙是常见的化合物,它们之间存在如下关系:若A为单质有色气体,请判断:(填化学式)

A是 ,B是 , C是 ,甲是 ,乙是 。
22.(10分)据2004年1月17日网易报道,意大利科学家使用普通氧分子和带正电的氧化离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子。
(1)下列有关O4的说法正确的是:
A.O4分子内存在极性共价键
B.合成O4的反应可看作核聚变反应,即不属于化学变化
C.O4与O3、O2都是氧的同素异形体
D.O4将来可用作更强有力的火箭推进的氧化剂
(2)制备含O2-、O22-甚至O2+的化合物都是可能的,通常它们是在氧分子进行下列各种反应时生成的:

上述反应中, (填序号)相当于氧分子的氧化; (填序号)相当于氧分子的还原。
(3)写出O22-的电子式:
(4)O2[PtF6]是一种含有O2+的化合物,请写出一种含有O2-的氧化物的化学式:__________________。
21.(8分)短周期元素的A、B、C在元素周期表中的位置如图所示,已知A、B、C三种元素的原子核外电子数之和等于B的质量数,B原子核内质子数和中子数相等。据此填空:
|
A |
|
C |
|
|
B |
|
(1)A的氢化物分子式为 ,分子构型为 ,属于 分子;
(2)B的元素符号为 ,原子结构示意图为 ,在周期表中位于第 周期族;
(3)C的单质分子式为 ,C的单质溶于水所得溶液叫 。
20、(6分)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物时,其电子式为 ,若XY2为共价化合物时,其形成过程的电子式为 。
19.(5分)有A、B、C、D、E五种微粒,其组成均有氢元素,且电子总数为10个,A是双原子的阴离子,它们之间能发生下列变化:
(1)A+B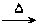 C+D↑(2)C+C
C+D↑(2)C+C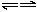 A+E(3)D+E
A+E(3)D+E B+C
B+C
由此可知它们的化学式分别为:
A ,B , C ,D ,E 。
18.同主族元素形成的同一类型化合物,往往其结构和性质相似。PH4I是一种白色晶体,下列对PH4I的叙述中,正确的是
A.它是一种共价化合物 B.它既含离子键又含共价键
C.它不可能与NaOH溶液反应 D.它受热时,可能会分解产生有色气体
17.已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,不正确的是
A.原子半径:X>Y>Z>W B.原子序数:Y>X>Z>W
C.原子最外层电子数:Y>X>Z>W D.金属性:X>Y,还原性:W2->Z-
16.下列叙述中,不正确的是
A.不同的原子之间只能构成共价化合物 B.单质中不一定存在非极性键
C.非金属原子之间只能构成共价化合物 D.Cl2的沸点比F2高,这与分子间作用力的大小有关
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com