
题目列表(包括答案和解析)
4、在FeCL3溶液中加入少量的铜粉,铜粉完全溶解,溶液颜色由棕黄色变成蓝绿色。
⑴推测并写出铜与FeCL3溶液反应的化学方程式: ;

 ⑵为了节省药品和时间,甲、乙两位同学用铜片、锌片、稀硫酸、CuSO4溶液、烧杯、试管等中学化学中常见的药品和仪器(用品),以“接力”式的方式,设计比较铜与锌还原性相对强弱的系列实验。试填写下列空白:①甲同学分别取一小片铜片、锌片置于烧杯底部(铜、锌不接触),小心地向烧杯中加入少量稀硫酸,观察到的现象是
,甲同学的设计思路是
;
⑵为了节省药品和时间,甲、乙两位同学用铜片、锌片、稀硫酸、CuSO4溶液、烧杯、试管等中学化学中常见的药品和仪器(用品),以“接力”式的方式,设计比较铜与锌还原性相对强弱的系列实验。试填写下列空白:①甲同学分别取一小片铜片、锌片置于烧杯底部(铜、锌不接触),小心地向烧杯中加入少量稀硫酸,观察到的现象是
,甲同学的设计思路是
;


 ②乙同学接着甲的实验,向烧杯中滴加
溶液,进而观察到的实验现象是
;乙同学得出锌、铜还原性相对强弱所依据的原理是
;
②乙同学接着甲的实验,向烧杯中滴加
溶液,进而观察到的实验现象是
;乙同学得出锌、铜还原性相对强弱所依据的原理是
;
 ③请你再单独设计一个简单的实验(试剂、仪器自选),探究和证实锌和铜还原性的相对强弱
③请你再单独设计一个简单的实验(试剂、仪器自选),探究和证实锌和铜还原性的相对强弱
3、 利用氧化还原反应和离子反应可以制备很多物质。例如,实验室以Zn、CuO、H2SO4为原料,可按下列两种途径 I :Zn
利用氧化还原反应和离子反应可以制备很多物质。例如,实验室以Zn、CuO、H2SO4为原料,可按下列两种途径 I :Zn 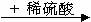 H2
H2 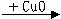 Cu
Cu
途径 II :CuO 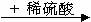 CuSO4
CuSO4 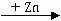 Cu
Cu
⑴写出有关反应的化学方程式:
途径I: ;途径II: ;

 ⑵若通过两种途径制得的等质量的Cu,下列说法正确的是
(填写序号)。
⑵若通过两种途径制得的等质量的Cu,下列说法正确的是
(填写序号)。
 ①消耗CuO的质量相等;②消耗Zn的质量相等;③消耗H2SO4的质量相等;
①消耗CuO的质量相等;②消耗Zn的质量相等;③消耗H2SO4的质量相等;
④生成ZnSO4的质量相等;⑤消耗H2SO4的质量不同;⑥途径I生成的ZnSO4较多。
2、 铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”。该绿锈俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],铜绿能跟酸反应生成铜盐及CO2和H2O。某同学利用下述系列反应实现了以下变化:铜
铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”。该绿锈俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],铜绿能跟酸反应生成铜盐及CO2和H2O。某同学利用下述系列反应实现了以下变化:铜
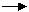 铜绿
铜绿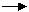 A
A 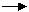 Cu(OH)2
Cu(OH)2 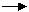 B
B 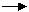 Cu
Cu
① ② ③ ④ ⑤
(已知B是一种易溶物质)
⑴上述反应中,属于复分解反应的是 (填序号),
 属于氧化还原反应的是
(填序号);
属于氧化还原反应的是
(填序号);
 ⑵写出反应①和⑤的化学方程式:①
;
⑵写出反应①和⑤的化学方程式:①
;
 ⑤
;(答案合理即可)
⑤
;(答案合理即可)
1、为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3)。碘酸钾和碘化钾在溶液中能发生下列反应:
5KI+KIO3+3H2SO4===3I2+3K2SO4+3H2O。
⑴该反应中,氧化剂是 ,还原剂是 ;

 ⑵当有1mol I2生成时,有 mol还原剂被氧化;
⑵当有1mol I2生成时,有 mol还原剂被氧化;
 ⑶当有1 mol氧化剂参与反应时,转移电子的总数为
mol 。
⑶当有1 mol氧化剂参与反应时,转移电子的总数为
mol 。
22、 (10分)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。已知水是反应的产物之一。
(10分)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。已知水是反应的产物之一。

 ⑴从硫和氮元素的价态看,只有氧化性的物质是
,只有还原性的物质是
,既有氧化性又有还原性的物质是
;
⑴从硫和氮元素的价态看,只有氧化性的物质是
,只有还原性的物质是
,既有氧化性又有还原性的物质是
;
 ⑵该反应中还原剂是
,氧化剂是
;
⑵该反应中还原剂是
,氧化剂是
;

 ⑶该反应中参与反应的H2S和HNO3的物质的量之比是
;
⑶该反应中参与反应的H2S和HNO3的物质的量之比是
;
 ⑷推测并写出反应的化学方程式
。
⑷推测并写出反应的化学方程式
。

B卷(拓展提高)
21、
 (8分)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
(8分)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
2Fe(NO3)3+16NaOH+3CL2===2Na2FeO4+6NaNO3+6NaCL+8H2O
⑴在上述反应中 元素被氧化,当3molCL2参与反应时,转移电子的总数为 ;

 ⑵铁酸钠之所以能净水,除了能消毒外,另一个原因是
。
⑵铁酸钠之所以能净水,除了能消毒外,另一个原因是
。
20、 (6分)在Fe、Fe2+、Fe3+、CL2、CL-、Na+几种粒子中,只有氧化性的是
,只有还原性的是
,既有氧化性又有还原性的是
。
(6分)在Fe、Fe2+、Fe3+、CL2、CL-、Na+几种粒子中,只有氧化性的是
,只有还原性的是
,既有氧化性又有还原性的是
。
18、
 (9分)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S===K2S+2NO2 +CO2 。其中被还原的元素是
,被氧化的元素是 ,氧化剂是
,还原剂是 ,
(9分)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S===K2S+2NO2 +CO2 。其中被还原的元素是
,被氧化的元素是 ,氧化剂是
,还原剂是 ,



 氧化产物是
,还原产物是
。
氧化产物是
,还原产物是
。
17.制取漂白液的化学方程式是:CL2+2NaOH===NaCL+NaCLO+H2O,该反应的氧化剂与还原剂的物质的量之比为:
A.1:1 B.1:2 C.2:1 D.3:2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com