
题目列表(包括答案和解析)
6. 下列物质在一定条件下不能发生水解的是 ( )
A.蔗糖 B.葡萄糖
C.蛋白质 D.油脂
5. 碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是
A.电池工作时,锌失去电子
B.电池工作时,电子由正极通过外电路流向负极
C.电池正极的电极反应式为:
2MnO2(s)+H2O(1)+2e-== Mn2O3(s)+2OH-(aq)
D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
4. 下列各分子中,所有原子都满足最外层为8电子结构的是
A H2O B BF3 C CCl4 D PCl5
3. 2008夏季奥运会将在我国举行,这次奥运会要突出“绿色奥运、科技奥运、人文奥运”的理念,其中“绿色奥运”是指
A.把环境保护作为奥运设施规划和建设的首要条件
B.严禁使用兴奋剂,使运动员公平竞争
C.所有奥运用品和食品全都是绿色的
D.奥运场馆建设均使用天然材料,不使用合成材料
2.面粉厂必须严禁烟火的主要原因是( )。
A.防止火灾发生
B.防止污染面粉
C.吸烟有害健康
D.面粉颗粒极小,当其扩散在空气中与空气充分接触,一旦引发反应,极易发生爆炸
1. 下列化学用语正确的是
A.碳-12原子 B.羟基的电子式
C.硫离子的结构示意图 D.乙烯的结构简式CH2CH2
22、某元素R的核外电子数等于核内中子数,2.8克该元素单质与氧气完全反应,可得到6克化合物RO2。
(1)该元素的原子的质量数为多少,是什么元素?
(2)如果把2.8克该元素单质投入到足量的氢氧化钠溶液中,生成的气体在标准状况下的体积是多少?
(三)为了使实验“定量化”、使结果更精确,可以对实验进行如下改进:
1.配制c(H+)相同的稀盐酸和稀硫酸:现有浓度为1mol·L-1的盐酸和密度为1.225g·cm-3、质量分数为20%的硫酸,若要准确量取该硫酸20.00mL,需要用⑤ (填仪器名称);将量取的硫酸配制成c(H+)=1mol·L-1的溶液,可得溶液的体积为⑥ 。
配制溶液时还需要用到的玻璃仪器有⑦ 、烧杯、胶头滴管和量筒等。
2.比较反应速率:反应时间可以用秒表测定。如果要对上述实验中的反应速率进行比较,可以通过测定哪些物理量来确定?要求回答一种即可。⑧ 。
21.(11分) 已知R表示烃基,R/表示烃基或氢原子,

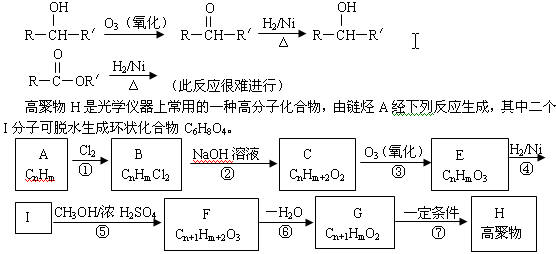
请回答下列问题:
(1)C6H8O4的结构简式是 。
(2)说明下列反应的类型:①是 反应;②是 反应;⑥是 反应。
(3)分别写出反应④、⑤和⑦的化学方程式(有机物用结构简式):
④ ;
⑤ ;
⑦ 。
(二)该同学取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
1.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
2.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验1中③ ,实验2中④ ,则说明原因Ⅲ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
(一)该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没有影响;
原因Ⅱ:① ;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻碍作用;
原因Ⅳ:Cl-、SO42-均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:②
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com