
题目列表(包括答案和解析)
5.关于化学键的下列叙述中,不正确的是
A、含有共价键的化合物一定是共价化合物
B、共价化合物中一定含有共价键
C、含有离子键的化合物一定是离子化合物
D、双原子单质分子中的共价键一定是非极性键
4.下列排列顺序正确的是:
A、半径:Al3+>Mg2+>Na+>F– B、稳定性:HI<HBr<HCl<HF
C、酸性:HClO4<H2SO4<H3PO4 D、碱性:Al(OH)3>Mg(OH)2>Ca(OH)2
2.人们把食品分为绿色食品、蓝色食品、白色食品等,绿色食品指通过光合作用转化的食品,海洋提供的食品叫做蓝色食品,通过微生物发酵制得的食品叫做白色食品,下面属于白色食品的是
A. 食醋 B. 面粉 C. 海带 D. 菜油
3下列化学用语的书写,正确的是
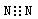 A、氮气的电子式:
B、次氯酸钙的化学式:Ca(ClO)2
A、氮气的电子式:
B、次氯酸钙的化学式:Ca(ClO)2
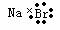 C、溴化钠的电子式:
D、乙醇的分子式:C2H5OH
C、溴化钠的电子式:
D、乙醇的分子式:C2H5OH
1.你认为减少酸雨不可采用的措施是
A、煤脱硫再作燃料 B、开发新能源
C、把工厂烟囱升高 D、多用风能、氢能、核能等
22. (6分)一定量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气重49.6克,当将其缓慢经过无水CaCl2时,CaCl2增重25.2克。则原混合气中CO2的质量为多少?
(6分)一定量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气重49.6克,当将其缓慢经过无水CaCl2时,CaCl2增重25.2克。则原混合气中CO2的质量为多少?



福建霞浦宏翔高级中学08-09学年第二学期第二次段考
21. (11分)如图是一位同学设计的实验室制取氯气的实验装置图。
(11分)如图是一位同学设计的实验室制取氯气的实验装置图。
 (1)写出该反应的化学方程式
;
(1)写出该反应的化学方程式
;
 (2)上述反应中,还原剂是
,若有1mol氧化剂参加反应,生成的氯气在标准状况下的体积为
L;
(2)上述反应中,还原剂是
,若有1mol氧化剂参加反应,生成的氯气在标准状况下的体积为
L;

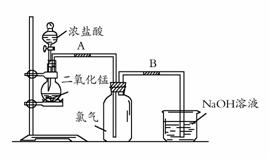 (3)实验开始前,某学生对装置进行了气密性检查。方法是:连接好装置后,用弹簧夹夹住 处(填"A"或"B")橡皮管;打开活塞向分液漏斗中加水,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中
时,表明该装置不漏气;
(3)实验开始前,某学生对装置进行了气密性检查。方法是:连接好装置后,用弹簧夹夹住 处(填"A"或"B")橡皮管;打开活塞向分液漏斗中加水,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中
时,表明该装置不漏气;
 (4)指出这套装置中存在的错误
(4)指出这套装置中存在的错误
 ;
;
 (5)烧杯里装有氢氧化钠溶液,其作用是
,发生反应的化学方程式是
(5)烧杯里装有氢氧化钠溶液,其作用是
,发生反应的化学方程式是
 。
。
20. (11分)短周期中的三种元素X、Y、Z,原子序数依次减小,原子核外电子层数之和是5,X元素原子的最外层电子数是Y和Z两元素原子的最外层电子数的总和;Y元素原子的最外层电子数是它的电子层数的2倍,且Y元素最高正价与最低负价的绝对值相等,X和Z可以形成XZ3的化合物。
(11分)短周期中的三种元素X、Y、Z,原子序数依次减小,原子核外电子层数之和是5,X元素原子的最外层电子数是Y和Z两元素原子的最外层电子数的总和;Y元素原子的最外层电子数是它的电子层数的2倍,且Y元素最高正价与最低负价的绝对值相等,X和Z可以形成XZ3的化合物。
 请回答:
请回答:
 (1)X、Y、Z三种元素的元素符号分别为X ,Y ,Z
;
(1)X、Y、Z三种元素的元素符号分别为X ,Y ,Z
;
 (2)元素X的原子得电子能力
(填"强于"或"弱于")元素Y的原子,可以用比较
(2)元素X的原子得电子能力
(填"强于"或"弱于")元素Y的原子,可以用比较
 的方法来判断;
的方法来判断;
 (3)XZ3的电子式是
,所含化学键类型是 ,属于
化合物;
(3)XZ3的电子式是
,所含化学键类型是 ,属于
化合物;
 (4)写出XZ3与Y的最高价氧化物的水化物按1∶1反应的化学方程式
(4)写出XZ3与Y的最高价氧化物的水化物按1∶1反应的化学方程式
 。
。
19. (4分)现有如下两个反应:
(4分)现有如下两个反应:
 (A)NaOH + HCl = NaCl + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(A)NaOH + HCl = NaCl + H2O
(B)2FeCl3 + Cu = 2FeCl2 + CuCl2
 ①根据两反应本质,判断能否设计成原电池 ;
①根据两反应本质,判断能否设计成原电池 ;
 ②如果不能,说明其原因 ;
②如果不能,说明其原因 ;
17. (10分)在银锌原电池中,以硫酸铜为电解质溶液,锌为
极,电极上发生的是
反应(填"氧化"或"还原"),电极反应式为 ;银为
极,电极上发生的是
反应(填"氧化"或"还原"),电极反应式
;银片上观察到的现象是
;当烧杯中溶液质量变化1g时,电路中有
mol电子通过。
(10分)在银锌原电池中,以硫酸铜为电解质溶液,锌为
极,电极上发生的是
反应(填"氧化"或"还原"),电极反应式为 ;银为
极,电极上发生的是
反应(填"氧化"或"还原"),电极反应式
;银片上观察到的现象是
;当烧杯中溶液质量变化1g时,电路中有
mol电子通过。
 18.(07年潍坊市期中考试,25)(10分)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:
18.(07年潍坊市期中考试,25)(10分)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,请回答:

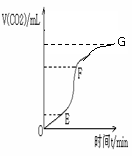 (1)实验过程如下图所示,分析判断:__ ______段化学反应速率最快,_______
段收集的二氧化碳气体最多。
(1)实验过程如下图所示,分析判断:__ ______段化学反应速率最快,_______
段收集的二氧化碳气体最多。
 (2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的
(2)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的
 是( )
是( )
 A.蒸馏水
B.氯化钠固体
A.蒸馏水
B.氯化钠固体
 C.氯化钠溶液
D.浓盐酸
C.氯化钠溶液
D.浓盐酸
 (3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?(至少回答两种)

 。
。
16.
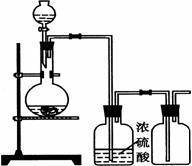 可用右图装置制取(必要时可加热)、净化、收集的气体是
可用右图装置制取(必要时可加热)、净化、收集的气体是
 A.铜和稀硝酸制一氧化氮
A.铜和稀硝酸制一氧化氮
 B.氯化钠与浓硫酸制氯化氢
B.氯化钠与浓硫酸制氯化氢
 C.锌和稀硫酸制氢气
C.锌和稀硫酸制氢气
 D.硫化亚铁与稀硫酸制硫化氢
D.硫化亚铁与稀硫酸制硫化氢







 福建霞浦宏翔高级中学08-09学年第二学期高二理科第二次段考
福建霞浦宏翔高级中学08-09学年第二学期高二理科第二次段考
 化学试题
化学试题
第Ⅱ卷(非选择题,共52分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com