
题目列表(包括答案和解析)
6. 元素性质呈周期性变化的根本原因是 ( )
A.元素的相对原子质量逐渐增大 B.核外电子排布的周期性变化
C.核电荷数逐渐增大 D.元素化合价呈周期性变化
5. A元素的最高正化合价和负化合价的绝对值之差为6,B元素和A元素的原子次外层上的电子数均为8,A与B可形成化合物BA2,则该化合物是( )
A. MgCl2 B. CaF2 C. SiO2 D. CS2
4.下列叙述中肯定A金属比B金属的活泼性强的是( )
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子的电子层数多
C.1molA从酸中置换出H+生成的H2比1molB从酸中置换出H+生成的H2多
D.常温时,A能从水中置换出氢,而B不能
3. 在核电荷数为1-18的元素的原子中,次外层电子数为最外层电子数2倍的元素有(
)
在核电荷数为1-18的元素的原子中,次外层电子数为最外层电子数2倍的元素有(
)
A.1种 B.2种 C.3种 D.4种
2.现有 bXn- 和 aYm+两种离子,它们的电子层结构相同,则与a相等的是( )
A. 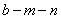 B.
B.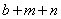 C.
C.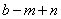 D.
D.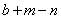
1.在化学反应中可能发生变化的是( )
 A.质子数 B.中子数 C.核外电子数 D.质量数
A.质子数 B.中子数 C.核外电子数 D.质量数
25(17分)实验室制取氯气时:
(1)所用仪器:-----------------------------------------------------------------------;
(2)反应原理:-----------------------------------------------------,该反应的还原剂是-----------;
(3)实验开始前要对装置进行------------,方法是-------------------------------------------;
(4)制取装置最后一部分用----------吸收多余气体,原因--------------,所发生的反应---------------------------------------------;能否用Na2CO3溶液吸收多余气体-----------(填能与否)
26. (9分)完成相关气体制备反应方程式:
(9分)完成相关气体制备反应方程式:
(1)氨气的实验室制备反应式:------------------------------------------------;
(2)二氧化碳的实验室制备反应式:------------------------------------------;
(3)氧气的实验室制备反应式:------------------------------------------------。

24.(16分)下表为元素周期表中的一部分,列出10种元素在元素周期表中的位置。试用元素符号、离子符号或化学式回答下列问题。
|
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
⑥ |
|
⑦ |
|
|
|
3 |
① |
③ |
⑤ |
|
⑧ |
|
⑨ |
⑩ |
|
4 |
② |
④ |
|
|
|
|
|
|
(1)10种元素中,化学性质最不活波的是-----------;(填元素符号)
(2)①③⑤三种元素最高价氧化物对应水化物中,碱性最强的是-----------;(填化学式)
(3)元素⑦的氢化物的化学式为--------;该氢化物常温下和元素②的单质反应的化学方程式------------------------------;
(4)①和⑧元素的最高价氧化物对应水化物的化学式为--------和------------;③和⑨两元素形成化合物的电子式------------;①和⑦两元素形成四核化合物的电子式------------,该物质与CO2反应的化学方程式-----------------------------------;
(5)①和⑤最高价氧化物对应水化物相互反应的离子方程式为------------------------------。
23.(10分)在下列事实中,什么因素影响了化学反应速率?
(1)黄铁矿煅烧时要粉碎成细小颗粒---------------------;
(2)夏天的食品易霉变,在冬天不易发生该现象-----------------------;
(3) 同浓度同体积的盐酸中放入同样大小的锌粒和镁块,产生气体有快有慢------------;
(4)同样大小的石灰石分别在0.1mol·L-1的盐酸和1mol·L-1的盐酸中反应速率不同-------------;
(5) 熔化的KClO3放出气泡很慢,撒入少量MnO2粉末后很快产生气体-----------------;
 21.(2分)有:①168O、178O、188O ②H2、D2、T2 ③O2、O3三组微粒或物质,回答下列问题(填编号):(1)互为同位素的是--------;(2)互为同素异形体的是---------。
21.(2分)有:①168O、178O、188O ②H2、D2、T2 ③O2、O3三组微粒或物质,回答下列问题(填编号):(1)互为同位素的是--------;(2)互为同素异形体的是---------。
22.(6分)X、Y、Z三种元素的离子结构都和Ar具有相同的电子层排布。H2在X单质中燃烧,产生苍白色火焰;Y元素的气态氢化物是H2Y,其最高价氧化物中Y的质量分数为40%;Z元素和N元素在同一族。
 (1)根据以上条件,推断X------,Y---------,Z------(填写元素符号);
(1)根据以上条件,推断X------,Y---------,Z------(填写元素符号);
(2)写出它们的最高价氧化物的水化物的化学式:X---------,Y---------,Z-----------。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com