
题目列表(包括答案和解析)
11.实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及其物质的量浓度,进行以下实验:
①量取25.00 mL甲溶液,向其中缓慢滴入乙溶液15.00 mL,共收集到224 mL(标准状况)气体。②量取15.00 mL乙溶液,向其中缓慢滴入甲溶液25.00 mL,共收集到112 mL(标准状况)气体。
(1)判断:甲是____ ____溶液,其物质的量浓度为 mol·L-1。
(2)实验②中所发生反应的离子方程式为_______________________ _____ 。
10. 2 L N2和CH4的混合气体与4 L O2点燃充分反应后,用干燥剂除去水分,剩余气体的体积为5 L。原来混合气体中N2和CH4的物质的量之比(各气体体积都在相同的温度、压强下测定)为
A.1:3 B.1:1 C.2:1 D.3:1
9. 有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)(单位: mol·L-1)为
A.(y-2x)/a B.(y-x)/a C.(2y-2x)/a D.(2y-4x)/a
8. 设NA表示阿伏加德罗常数,下列说法正确的是
①  6.8g熔融的KHSO4中含有0.1Na个阳离子。
6.8g熔融的KHSO4中含有0.1Na个阳离子。
② 1L1mol/L的盐酸溶液中,含HCl分子数为1Na。
③ 常温常压下,11.2L的CH4中含有的H数为2Na。
④ 0.1molNa2O2与水完全反应,转移0.2NA的电子。
⑤  62gNa2O溶于水中,所得溶液中有1Na个O2-
62gNa2O溶于水中,所得溶液中有1Na个O2-
⑥ 1L1mol/L的醋酸溶液中离子总数为2Na
⑦ 标准状况下,22.4L氩气含有原子数为2Na。
⑧ 常温常压下,32gO2、O3的混合物含有2Na个氧原子。
⑨ 1L1mol/L的酒精溶液,含有1Na个分子。
⑩1molFe和足量的盐酸反应,失去3Na个电子。
A.①②⑤⑦⑧ B.②④⑥⑧⑩ C .⑧⑩ D .⑧
7.下列说法正确的是
A.把100mL3mol·L-1的H2SO4跟100mLH2O混合,硫酸的物质的量浓度改变为1.5mol·L-1
B.把100g20%的NaCl溶液跟100gH2O混合后,NaCl溶液的质量分数是10%
C.把200mL3mol·L-1的BaCl2溶液跟100mL3mol·L-1的KCl溶液混合后,溶液中的C(Cl-)仍然是3mol·L-1
D.已知某温度KNO3的溶解度是31.6g,该温度下将20gKNO3溶解于50g水中,充分溶解,获得溶液的质量分数是28.6%
6.下列叙述的两个量,一定相等的是
A.0.1mol·L-1NaCl与0.05mol·L-1Na2CO3溶液中的Na+离子数目
B.质量相等的金刚石和C60中的碳原子数目
C.标准状况下等体积的SO2与SO3的分子数目
D.pH都为3的稀盐酸与FeCl3溶液中,由水电离产生的H+离子数目
5.将标准状况下的某气体(摩尔质量为Mg•mol-1)溶于ag水中,所得到溶液的密度为bg•cm-3,物质的量浓度为cmol•L-1,则该气体溶入水中的体积是 ( )
A.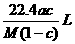 B.
B.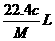 C.
C.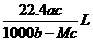 D.
D.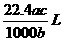
4.用98%的浓H2SO4(密度为1.84g/ml)配制的1mol·L-1的稀H2SO4100ml,配制过程中可能用到下列仪器:①100mL量筒;②10mL量筒;③50mL烧杯;④托盘天平;⑤100mL容量瓶;⑥胶头滴管;⑦玻璃棒,按使用出现的先后顺序排列正确的是 ( )
A.②⑥③⑦⑤ B.④③⑤⑦⑥ C.①③⑦⑤⑥ D.②⑤⑦⑥
3. 足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·mol-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是 ( )
A.60mL B.45mL C.30mL D.15mL
2.在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿佛加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为 ( )
A.2mol·L-1 B.2.5 mol·L-1
C.5 mol·L-1 D.7.5 mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com