
题目列表(包括答案和解析)
13.
 一定温度下,可逆反应3X(g)+Y(g) 2Z(g)达到限度的标志是
( )
一定温度下,可逆反应3X(g)+Y(g) 2Z(g)达到限度的标志是
( )
A.单位时间内生成3n mol X,同时消耗n mol Y B.X的生成速率与Z的生成速率相等
C.X、Y、Z的浓度相等 D.X、Y、Z的分子个数比为3:1:2
12. 在10℃时某化学反应速率为0.1 mol/(L•s),若温度每升高10℃反应速率增加到原来的2倍。为了把该反应速率提高到1.6 mol/(L•s),该反应需在什么温度下进行?( )
A. 30℃ B. 40℃ C. 50℃ D. 60℃
⒈ 绿色能源是指使用过程中不排放或排放极少污染物的能源,如一级能源中的水能、地热、天然气等;二级能源中电能、氢能等。下列能源属于绿色能源的是 ( )
① 太阳能 ② 风能 ③ 石油 ④ 煤 ⑤ 潮汐能 ⑥ 木材
A.①②③ B.③④⑤ C.④⑤⑥ D.①②⑤
⒉ 已知中和热的数值是57.3 kJ·mol–1。下列物质反应时,产生57.3 kJ热量的是( )
A.稀HCl和稀NaOH
B.1.0 mol·L-1 HCl和1.0 mol·L –1 NaOH
C.500 mL 2.0 mol·L-1 HCl和500 mL2.0 mol·L –1 NaOH
D.500 mL 2.0 mol·L-1 H2SO4和500 mL 2.0 mol·L-1 Ba(OH)2
⒊ 下列说法正确的是 ( )
 A.由H原子形成1
mol H-H键要吸收热量
A.由H原子形成1
mol H-H键要吸收热量
B.所有燃烧反应都是放热反应
C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O时所释放的热量称为中和热
D.凡经加热而发生的化学反应都是吸热反应
⒋ 实验室中制取氢气,最好的方法是( )。
A.纯锌与稀硫酸反应 B.纯锌与浓硫酸反应
C.纯锌与稀盐酸反应 D.粗锌(含铜、银)与稀硫酸反应
⒌ 据报道,锌电池可能取代目前广泛应用的铅蓄电池,因为锌电池容量更大,而且没有铅污染。其电池反应为:2Zn+02=2ZnO,原料为锌粒、电解质和空气,则下列叙述正确的是( )。
A.锌为正极,空气进入负极反应 B.负极反应为Zn-2e-=Zn2+
C.正极发生氧化反应 D.电解液肯定不是强酸
⒍ 右图是氢氧燃料电池构造示意图。关于该电池说法不正确( )
A.a极是负极
B.正极的电极反应是:O2+2H2O+4e-=4OH-
C.电子由b通过灯泡流向a
D.氢氧燃料电池是环保电池
⒎ 铁在下列情况下腐蚀最快的是 ( )
A.铁放入海水中
B.将铁和锌连接后放入到海水中
 C.将铁和锌连接后放入到淡水中
C.将铁和锌连接后放入到淡水中
D.将铁和锡连接后放入到海水中
⒏ 锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。 某种锂电池的总反应式是Li+MnO2 = LiMnO2。下列说法正确的是( )
A. Li是负极,电极反应为Li-e-=Li+
B. Li是正极,电极反应为Li+e-=Li-
C. MnO2是负极,电极反应为MnO2+e-=MnO2-
D. 锂电池是一种环保型电池
⒐ 在m A + n B  p C的反应中,m、n、p为各物质的计量数。现测得C每分钟增加a
mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a
mol/L,则m:n:p为 ( )
p C的反应中,m、n、p为各物质的计量数。现测得C每分钟增加a
mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a
mol/L,则m:n:p为 ( )
 A. 2:3:2 B.
2:3:3 C.
1:3:2 D.
3:1:2
A. 2:3:2 B.
2:3:3 C.
1:3:2 D.
3:1:2
10. 可逆反应H2(g)+I2(g) 2HI(g)达到平衡状态时的标志是 ( )
A. 混合气体的体积恒定不变 B. 混合气体的颜色不再改变
C. H2、I2、HI的浓度相等 D. I2在混合气体中的体积分数与H2在混合气体中的体积分数
⒒ 根据下列事实:①X+Y2+=X2++Y;②Z+H2O(冷)=Z(OH)2+H2↑;③Z2+氧化性比X2+弱;④由Y、W电极组成的电池,电极反应为W2++2e-=W、Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序为 ( )
A. X > Z > Y > W B. Z > W > X > Y C. Z > Y > X > W D. Z > X > Y > W
20. 一些盐的结晶水合物,在温度不太高时就有熔化现象,既熔溶于自身的结晶水中,又同时吸收热量,它们在塑料袋中经日晒能熔化,在日落后又可缓慢凝结而释放热量,用以调节室温,称为潜热材料。现有几种盐的水合晶体有关数据如下:
|
|
Na2S2O3·5H2O |
CaCl2·6H2O |
Na2SO4·10H2O |
Na2HPO4·12H2O |
|
熔点℃ |
40~50 |
29.92 |
32.38 |
35.1 |
|
熔化热(kJ/相对分子质量) |
49.7 |
37.3 |
77.0 |
100.1 |
(1)上述潜热材料中最适宜应用的两种盐是______、________________。
(2)实际应用时最常用的(根据来源和成本考虑)应该是_____________。
19.目前大部分城市居民所使用的燃料主要是管道煤气,使用天然气作为居用燃料对环境更为有利。管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4。它们的燃烧反应如下:
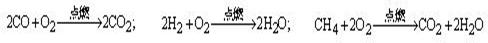
根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是_________。因此燃烧管道煤气的灶具如需改烧天然气,灶具的改进方法是_________进风口(填增大或减小),如不作改进可能产生的不良结果是_________________。管道煤气中含有的烃类,除甲烷外,还有少量乙烷、丁烷等,它们的某些性质见下表:

试根据以上某个关键数据解释冬天严寒的季节有时管道煤气火焰很小,并且呈断续状态的原因是 _______________________。
18. 2008年我国成功回收“神舟七号”载人飞船,这标志着“我国的载人航天事业又迈出了新的重要一步”:
⑴飞船返回时,由于与大气层的剧烈摩擦,产生高温。为了防止飞船温度过高,在飞船表面涂上一种特殊的涂料,该涂料的性质最可能的是 A.在高温下不融化 B.在高温下可分解气化
C.在常温下就分解气化 D.该涂料不可能发生分解
(2)火箭升空需要高能的燃料,肼(N2H4)是发射航天飞船常用的高能燃料。一般将液态N2O4作为火箭的推进剂。已知1mol液态肼与足量液态N2O4完全反应放出QkJ的热量,产物是对环境无害的氮气和水蒸气。写出该反应的热化学方程式 。该反应中被氧化的原子与被还原的原子物质的量之比是 。但实际发射过程中会看到有大量红色的烟雾,除了该反应可能产生少量NO外,产生此现象的原因可能是 。
(3)实际上,最理想的燃料是燃烧热大、体积小、本身毒性小、安全的固态氢,目前人们还不能制得固态氢,因为 。
(4)飞船返回时,对宇航员要进行严格的体检。人体血液的pH变化范围较小,pH只能在7.0-7.8的范围内变化,否则将会有生命危险。实验证明,在50mL的血液中加入1滴(0.05mL)10mol/L的盐酸时,pH由7.4降至7.2,如果向50mL、pH为7.4的NaOH溶液中加入1滴(0.05mL)10mol/L盐酸时,pH大约将变为 。显然,人体血液具有 的作用。
16.已知1mol CO气体完全燃烧生成CO2气体,放出283KJ热量,1mol氢气完全燃烧生成液态水放出286KJ热量,1mol CH4气体完全燃烧生成CO2气体和液态水放出890KJ热
 ⑴ 写出H2完全燃烧热化学方程式
⑴ 写出H2完全燃烧热化学方程式
⑵ 若1mol CH4气体完全燃烧生成CO2气体和水蒸汽,放出热量 890KJ(填“ =”、“>””<”)
⑶ 若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和水蒸汽,则放出热量(Q)的取值范围是
⑷若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和水蒸汽,且CO2和H2O物质的量相等,则放出热量(Q)的取值范围是
15.CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是 。
(2)已知在101 kPa时,CO的燃烧热为283 kJ/mol。相同条件下,若2 molCH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30 倍,CH4完全燃烧反应的热化学方程式是: 。
(3)120℃、101 kPa下,a mL由CO、CH4组成的混合气体在bmL O2中完全燃烧后,恢复到原温度和压强。①若混合气体与O2恰好完全反应,产生b mLCO2,则混合气体中CH4的体积分数为 (保留2位小数)。② 若燃烧后气体体积缩小了a/4 mL ,则a与b关系的数学表示式是 。
14.在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氧气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出肼和过氧化氢的结构式:肼___________________,过氧化氢______________ 。
(2)写出热化学方程式_________________________________________________。
(3)已知H2O(1)==H2O(g) △H=+44kJ/mol,则16g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是_____________________ kJ。
(4)上述反应用于火箭推进剂,除释放大量热和快速产生大量气体外,还有一个很突出的优点是_______________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com