
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
4°¢∏˘æ𜬡–∑¥”¶≈–∂œ”–πÿŒÔ÷ ªπ‘≠–‘”…«øµΩ»ıµƒÀ≥–Ú «(°°°° ) °°°°°°°°°°°°°°°°
H2SO3+I2+H2O====2HI+H2SO4°°°° 2FeCl3+2HI====2FeCl2+2HCl+I2
3FeCl2+4HNO3====2FeCl3+NO°¸+2H2O+Fe(NO3)3
A£Æ H2SO3£æI-£æFe2+£æNO°°°°°°°°°°°° B£Æ I-£æFe2+£æH2SO3£æNO
C£Æ Fe2+£æI-£æH2SO3£æNO°°°°°°°°°°°° D£Æ NO£æFe2+£æH2SO3£æI-
3°¢‘⁄xR2++yH++O2=MR3++nH2Oµƒ¿Î◊”∑Ω≥à Ω÷–£¨∂‘œµ ˝m∫ÕR3+µƒ≈–∂œ’˝»∑µƒ «(°°°° )
A£Æm=4°°°° R3+ «—ıªØ≤˙ŒÔ°°°°°°°°°°°°°° B£Æm=3°°°° R3+ «ªπ‘≠≤˙ŒÔ
C£Æm=2°°°° R3+ «—ıªØ≤˙ŒÔ°°°°°°°°°° °°°°°°D£Æm=y°°°° R3+ «ªπ‘≠≤˙ŒÔ
2°¢œ¬¡–±‰ªØ£¨–Ë“™º”»Î µ±µƒ—ıªØº¡≤≈ƒÐÕÍ≥…µƒ «(°°°° ) °°
°°
A£ÆCuO°˙Cu°°°°°°°°°°°°°°°°°°°° B£ÆFe°˙FeCl2°°
C£ÆH2SO4°˙CuSO4 °°°°°°°°°°°°°°°°D£ÆHNO3°˙NO2
1°¢œ¬¡–∑¥”¶÷–£¨ÀÆ◊ˆ—ıªØº¡µƒ «(°°°° )
A£ÆCl2+H2O=HCl+HClO°°°°°°°° B£ÆC+H2O CO+H2
CO+H2
C£ÆCaO+H2O=Ca(OH)2°°°°°°°° D£ÆCO2+H2O=H2CO3
34£Æ(4∑÷)“—÷™∑¥”¶£∫3Cl2+8NH3=N2+6NH4Cl
»Ù71gCl2≤Œº”∑¥”¶±ª—ıªØµƒNH3µƒ÷ ¡øŒ™∂ý…Ÿ£øªπ‘≠≤˙ŒÔµƒ÷ ¡øŒ™∂ý…Ÿ£ø(11.3g°° 107g)

°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °˜
33£Æ(6∑÷)“—÷™Õ≠”Î≈®¡ÚÀ·µƒ∑¥”¶Œ™ Cu +2H2SO4(≈®)°° = CuSO4+SO2°¸+2H2O£¨µ±∑¥”¶÷–…˙≥…32øÀSO2∆¯Ã ±£¨œ˚∫ƒH2SO4µƒ÷ ¡ø «∂ý…ŸøÀ£ø∆‰÷–”–∂ý…ŸøÀH2SO4◊˜Œ™—ıªØº¡±ªªπ‘≠£ø
(98øÀ£¨49øÀ)
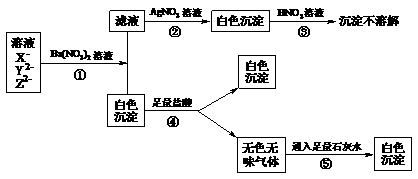
32£Æƒ≥»Ð“∫÷–∫¨”–X-°¢Y2-°¢Z2-»˝÷÷≥£º˚µƒŒÞª˙¿Î◊”°£»Áœ¬ÕºøÚÕºÀ˘ 棨∑¢…˙¡À“ªœµ¡–ªØ—ß∑¥”¶°£µ⁄¢Ð≤Ω∑¥”¶…˙≥…µƒ∞◊…´≥¡µÌ÷–∫¨Y2-.
|
|
|||||
|
||||||
|
|
°°¢≈≈–∂œX-°¢Y2-°¢Z2-∑÷±Œ™________°¢________°¢________(–¥¿Î◊”∑˚∫≈)°£
°°¢∆–¥≥ˆ¢Ÿ°¢¢⁄°¢¢Ð°¢¢ð≤Ω∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω°£
°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°
°¢¢≈Cl-°¢SO42-°¢CO32- (√øø’1∑÷) ¢∆¢ŸSO42-+Ba2+==BaSO4°˝°° CO32-+Ba2+==BaCO3°˝°°
¢⁄Ag++Cl-==AgCl°˝°° ¢ÐBaCO3+2H+==Ba2++CO2°¸+H2O°°
¢ðCa2++2OH-+CO2==CaCO3°˝+H2O (√ø∏ˆ¿Î◊”∑Ω≥à Ω2∑÷)
30£Æ≥˝»•¿®∫≈÷–‘”÷ £¨–¥≥ˆÀ˘º” ‘º¡”Î∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω°£
°°°° ¢≈ Cl-(SO42-)£¨À˘º” ‘º¡£∫BaCl2 _________£¨¿Î◊”∑Ω≥Ã Ω£∫___________________________°£
°°°° ¢∆CO2(HCl)£¨À˘º” ‘º¡£∫NaHCO3 _________£¨¿Î◊”∑Ω≥Ã Ω£∫___________________________°£
°° 31£Æ‘⁄“ª…’±≠÷– ¢”–œ°H2SO4»Ð“∫£¨Õ¨ ±”–“ª±Ì√Êπ‚ª¨µƒÀСœ–°«Ú–¸∏°°°°°
31£Æ‘⁄“ª…’±≠÷– ¢”–œ°H2SO4»Ð“∫£¨Õ¨ ±”–“ª±Ì√Êπ‚ª¨µƒÀСœ–°«Ú–¸∏°°°°°
”⁄»Ð“∫÷–—Î(»ÁÕºÀ˘ æ)°£œÚ∏√…’±≠¿Ôª∫ª∫◊¢»Î”Îœ°H2SO4µ»√Ð∂»µƒ°°
Ba(OH)2»Ð“∫÷¡«°∫√ÕÍ»´∑¥”¶°£‘⁄¥À µ—Èπ˝≥Ã÷–
°°°° ¢≈…’±≠¿Ôπ€≤ÏµΩµƒ µ—Èœ÷œÛ”–£∫
°°°°°° ¢Ÿ____________________________________________£¨
°°°°°° ¢⁄____________________________________________°£
¢∆–¥≥ˆ µ—Èπ˝≥Ã÷–∑¥”¶µƒ¿Î◊”∑Ω≥à Ω________________________________________°£
¢≈¢Ÿ≤˙…˙∞◊…´≥¡µÌ°° ¢⁄–°«Úœ¬≥¡°° ¢∆Ba2++2OH-+2H++SO42-==BaSO4°˝+2H2O (¿Î◊”∑Ω≥à Ω2∑÷)
29.«Î∏˘æð∑¥”¶¢ŸX2+2Z-£Ω2X-+Z2 °°°°°°°°°°°°¢⁄Z2+2W-£Ω2Z-+W2 °°°°°°°°°°°°¢€W2+2Y-£Ω2W-+Y2°°≈–∂œ£∫ (1)ƒƒ–©ŒÔ÷ æþ”–—ıªØ–‘£¨≤¢÷∏≥ˆ—ıªØƒÐ¡¶«ø»ıÀ≥–Ú°£ ___________ _____________ X2>Z2>W2>Y2_____________________________________________ (2)∑¥”¶W2+2X-£Ω2W-+X2ƒÐ∑ÒΩ¯––£¨Àµ√˜¿Ì”…°£ _____________ _W2≤ªƒÐΩ´X-—ıªØ___________________________________ ________________
28£Æ(4∑÷)œ÷”–“‘œ¬ŒÔ÷ £∫¢ŸKClæßð° ¢⁄“∫èHCl ¢€¥◊À·°° ¢ÐπØ°° ¢ðCaCO3πÃÃÂ
¢Þœ°¡ÚÀ·°° ¢þæ∆æ´(C2H5OH)°° ¢ý“∫èKNO3£¨¢·“∫èSO3«Îªÿ¥œ¬¡–Œ Â(”√–Ú∫≈)£∫
°°°° ¢≈“‘…œŒÔ÷ ÷–ƒÐµºµÁµƒ «_¢Ð¢Þ¢ý________________°£
°°°° ¢∆“‘…œŒÔ÷ ÷– Ù”⁄µÁΩ‚÷ µƒ «_____¢Ÿ¢⁄¢€¢ð¢ý______________°£
°°°° ¢«“‘…œŒÔ÷ ÷– Ù”⁄∑«µÁΩ‚÷ µƒ «____¢þ ¢·________________°£
°°°° ¢»“‘…œŒÔ÷ ÷–»Ð”⁄ÀÆ∫Û–Œ≥…µƒÀƻГ∫ƒÐµºµÁµƒ «_¢Ÿ¢⁄¢€¢Þ¢ý¢·°° ___________________°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com