
题目列表(包括答案和解析)
2. 需加入适当的还原剂才能实现的反应是( )
A、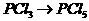 B、
B、 C、
C、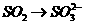 D、
D、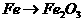
3一种强酸溶液的导电能力与一种弱酸溶液的导电能力的大小关系是( )
A、大于 B、小于 C、等于 D、不能肯定
1.下列说法正确的是( )
A、置换反应一定属于氧化还原反应 B、分解反应均不属于氧化还原反应
C、复分解反应有的属于氧化还原反应 D、化合反应一定属于氧化还原反应
22.(8分)
(1)6 mol/L的HCl溶液100mL可稀释成0.6mol/L的HCl溶液多少毫升?
(2)有未知浓度的碳酸钠溶液200mL,加入过量的上述盐酸能生成CO2气体5.6 L(标准状况)。计算原碳酸钠溶液中Na2CO3的物质的量浓度。
2009-2010学年度第一学期高中教学质量监测(一)
21. (14分)为除去粗盐中的Ca2+、Mg2+、SO42- 以及泥沙等杂质,某同学设计了
(14分)为除去粗盐中的Ca2+、Mg2+、SO42- 以及泥沙等杂质,某同学设计了
 一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)

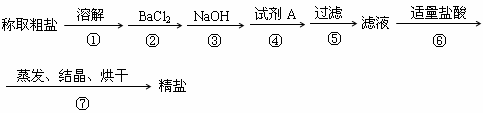
 (1)试剂A为
(填化学式)
(1)试剂A为
(填化学式)
 (2)判断BaCl2已过量的方法是
。
(2)判断BaCl2已过量的方法是
。

 (3)第③步中,写出相应的化学方程式
。
(3)第③步中,写出相应的化学方程式
。
 (4)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
。
(4)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
。
 (5)过滤需用滤纸、铁架台(带铁圈),还需用到的仪器有 。
(5)过滤需用滤纸、铁架台(带铁圈),还需用到的仪器有 。
 (6)为检验精盐纯度,需配制250 mL 0.2 mol/L NaCl(精盐)溶液,
(6)为检验精盐纯度,需配制250 mL 0.2 mol/L NaCl(精盐)溶液,
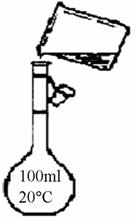
 题图是该同学转移溶液的示意图,图中的错误是
题图是该同学转移溶液的示意图,图中的错误是
 ① 、
① 、
 ② 。
② 。
20. (9分)
(9分)
 (1)为检验某溶液中是否含有SO42-离子,所需试剂为
;其最佳操作顺序为:
(1)为检验某溶液中是否含有SO42-离子,所需试剂为
;其最佳操作顺序为:
 ①先加入
,现象:
;
①先加入
,现象:
;
 ②后加入
,现象:
。
②后加入
,现象:
。
 (2)某KNO3溶液中含有少量K2SO4 ,为完全除去SO42-得到纯净的KNO3溶液,所需试剂
(2)某KNO3溶液中含有少量K2SO4 ,为完全除去SO42-得到纯净的KNO3溶液,所需试剂
 为
。
为
。
19. 质量分数为a%的浓盐酸,其密度为b g/mL。试计算:100mL这种溶液中,所含HCl的质量为 、HCl的物质的量为 。
质量分数为a%的浓盐酸,其密度为b g/mL。试计算:100mL这种溶液中,所含HCl的质量为 、HCl的物质的量为 。
18. (1)将100mL0.1mol/L的NaCl溶液和100mL0.5mol/L的CaCl2溶液混合后,若溶液的总体积为二者体积之和,则混合溶液中c (Cl-)为 mol/L 。
(1)将100mL0.1mol/L的NaCl溶液和100mL0.5mol/L的CaCl2溶液混合后,若溶液的总体积为二者体积之和,则混合溶液中c (Cl-)为 mol/L 。
 (2)V L Fe2 (SO4)3溶液中含Fe3+ m g ,则该溶液中SO42-的物质的量浓度为
mol/L,Fe2
(SO4)3的物质的量浓度为 mol/L 。
(2)V L Fe2 (SO4)3溶液中含Fe3+ m g ,则该溶液中SO42-的物质的量浓度为
mol/L,Fe2
(SO4)3的物质的量浓度为 mol/L 。
17. (1)在标准状况下,112mL某气体的质量是0.28g ,则这种气体的相对分子质量为
,摩尔质量为
。
(1)在标准状况下,112mL某气体的质量是0.28g ,则这种气体的相对分子质量为
,摩尔质量为
。
 (2)在同温同压下,气体A的密度是氢气密度的15倍,则气体A的相对分子质量为
。
(2)在同温同压下,气体A的密度是氢气密度的15倍,则气体A的相对分子质量为
。
16. 0.5molNH3分子中含有
个NH3分子,
个H原子;NH3的质量为 g,标准状况下的体积为 L 。
0.5molNH3分子中含有
个NH3分子,
个H原子;NH3的质量为 g,标准状况下的体积为 L 。
15. 如果a g某气体中所含有的分子数为b, 则c
g该气体在标准状况下的体积是
如果a g某气体中所含有的分子数为b, 则c
g该气体在标准状况下的体积是
 (式中NA为阿伏加德罗常数)
(式中NA为阿伏加德罗常数)
 A.22.4bc/aNA
L B. 22.4ab/cNA L C.22.4ac/ bNA L D. 22.4b/acNA
L
A.22.4bc/aNA
L B. 22.4ab/cNA L C.22.4ac/ bNA L D. 22.4b/acNA
L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com