
题目列表(包括答案和解析)
6.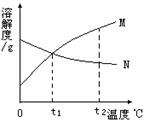 右图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是
右图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是
A.t2℃时,M、N两物质溶液溶质质量分数相等
B.由t1℃升温到t2℃时,N物质溶液溶质质量分数不变
C.M物质的溶解度大于N物质的溶解度
D.N物质的溶解度随温度的升高而降低
5.某化学兴趣小组欲用溶解过滤的方法分离下列混合物,其中不适宜用此法分离的一组是
A.碳酸钙 碳酸钠 B.氯化钙 氯化银 C.硝酸钙 硝酸银 D.氢氧化钠 氢氧化铜
4.复印材料时,经常能闻到一股特殊的气味,这种气味就是臭氧(O3)的气味。氧气在放电条件下可以转化为臭氧。下列与此相关的说法中正确的是:
A.该变化是物理变化 B.同种元素可组成不同的单质
C.臭氧与氧气是同一种物质 D.臭氧与氧气性质完全相同
3.分子、原子、离子都是构成物质的粒子。下列有关说法正确的是
A.原子是不可再分的粒子
B.氯化钠是由氯化钠离子构成的
C.“丹桂飘香”可以说明分子间有间隔
D.蒸馏水与海水中的水的化学性质相同
2.下列物质的用途主要与其化学性质相关的是
A.干冰用于人工降雨 B.石墨可用作干电池的电极
C.用生石灰作某些食品的干燥剂 D.用钨作灯泡中的灯丝
1.成语被誉为中华民族语言的瑰宝。下列成语中,其本意主要为化学变化的是
A.磨杵成针 B.木已成舟 C. 积土成山 D.死灰复燃
32.黄铜(由锌和铜形成的合金)有较强的耐磨性能在生活中有广泛的用途,晓军同学为了测定黄铜屑样品组成,分四次取样品与稀硫酸反应,其实验数据记录如下表:
|
|
1 |
2 |
3 |
4 |
|
样品质量/g |
25.0 |
25.0 |
25.0 |
25.0 |
|
稀硫酸质量/g |
40 |
80 |
120 |
160 |
|
产生气体质量/g |
0.2 |
0.4 |
0.5 |
0.5 |
计算:(1)黄铜样品中铜的质量;(2)所用稀硫酸中溶质质量分数。
31.(4分)某活动小组的同学查阅资料得知,传统腌制松花蛋的主要配料是氧化钙、纯碱和食盐。小组同学将这三种物质混合后加入适量的水搅拌,过滤得滤渣和滤液,对滤液中溶质的成分进行探究:
[猜想与假设] 甲同学认为:可能是NaCl、Na2CO3、Ca(OH)2
乙同学认为:可能是NaCl、NaOH、Na2CO3
丙同学认为:可能是NaCl、NaOH、Ca(OH)2
丁同学认为:可能是NaCl、NaOH
[交流与评价] 经过讨论,大家一致认为 同学的猜想不合理。其理由是 。
[活动与探究] (1)乙同学取原滤液向其中倾倒一定量的稀盐酸观察到有大量气泡产生,于是得出该滤液中的溶质是NaCl、NaOH、Na2CO3的结论,证实了自己的猜想。
(2)丙同学取原滤液向其中加入Na2CO3溶液无现象,据此否定了自己的猜想;他又重新取原滤液,向其中加入CaCl2溶液观察到 ,得出了和乙同学相同的结论。
(3)丁同学为了验证上述结论也取原滤液向其中滴加了少量稀盐酸,却发现无气泡产生。
[解释与结论] 大家经过分析找出了丁同学所用试剂与乙同学相同,却没有看到气泡的原因。你认为可能的原因是 。经过上述四位同学的共同努力,大家终于对滤液中溶质的成分得出了正确结论。
30.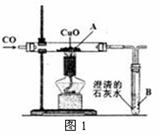 (7分)Ⅰ.小明设计了右图1所示的实验装置,进行一氧化碳还原氧化铜的实验。试回答:
(7分)Ⅰ.小明设计了右图1所示的实验装置,进行一氧化碳还原氧化铜的实验。试回答:
(1)该装置的不足之处是 。
(2)实验开始时,先要进行的操作是 (填序号:①加热②
通一氧化碳)。
(3)实验过程中,A处反应的化学方程式是 。
Ⅱ.为分离A装置中反应排出的一氧化碳和二氧化碳,小明又设计
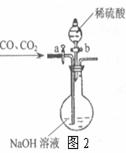 了右图2所示的装置(铁架台、铁夹等固定用装置已略去,a、b
了右图2所示的装置(铁架台、铁夹等固定用装置已略去,a、b
为活塞)。
(1)当关闭活塞b,打开活塞a时,可分离得到 。
(2)然后关闭活塞a,再打开活塞b,可分离得到 。
Ⅲ.对于A装置中反应后得到的红色固体(此时氧化铜已全部反应完),
小明进行了以下探究。
[查阅资料]①氧化铜经一氧化碳还原不仅能生成铜,还可能生成中间产物氧化亚铜(化学式为Cu2O)。
②Cu2O是不溶于水的红色固体,在酸性溶液中,可发生反应生成Cu2+和Cu。
[提出猜想]氧化铜经一氧化碳还原所得到的红色固体中除Cu外还可能含有Cu2O。
[进行实验]小明设计了下列实验方案,请填写完整。
|
实验步骤 |
|
|
实验现象与结论 |
|
29.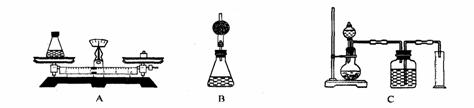 (5分)甲、乙、丙三位学生为了测定H2O2溶液中溶质的质量分数,先测定H2O2完全分解时产生氧气的质量,然后计算出H2O2溶液中溶质的质量分数,他们所取的双氧水溶液的质量相等。
(5分)甲、乙、丙三位学生为了测定H2O2溶液中溶质的质量分数,先测定H2O2完全分解时产生氧气的质量,然后计算出H2O2溶液中溶质的质量分数,他们所取的双氧水溶液的质量相等。
(1)甲同学首先设计图A的装置,向装有样品溶液20 g的锥形瓶(瓶重75 g)中加入0.5gMnO2,待双氧水反应完毕后测得锥形瓶和反应后混合物总质量为95.1g,则产生氧气的质量是_________g,双氧水溶液的溶质质量分数是_________%。
(2)乙同学认为甲的实验有误差,他设计了如图B的装置(只在甲方案的锥形瓶上加一个盛生石灰的干燥管,其他所用仪器和操作与甲相同),他认为甲实验有误差的理由是______________________________________________________________。
(3)丙认为甲、乙学生用称量法测定实验误差都较大,其理由是____________________
___________________________________________,设计了如图C的实验装置图,先测生成氧气的体积,再求生成氧气的质量(常温下氧气密度为1.42 g/L)。要满足丙的要求,该实验中所用量筒应是下列规格中的__________(填序号)。
A.100mL B.250 mL C.500 mL D.10 mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com