
题目列表(包括答案和解析)
6.二氧化硫是污染大气并形成酸雨的主要有害物质之一。造成大气中二氧化硫含量急剧增加的最主要原因是
A.硫酸厂排放出的废气中的二氧化硫
B.由火山爆发产生的二氧化硫
C.由实验室逸出的二氧化硫
D.由煤和石油燃烧产生的二氧化硫
5.实验室用的坩埚和蒸发皿属于
A.玻璃类 B.陶瓷类
C.新型无机非金属材料 D.以上都不是
4.含有非极性键的离子化合物是
A.Na2O2 B.NaOH C.NH4Cl D.H2O2
3.同周期的A、B、C三种元素,其最高价氧化物对应水化物的酸性强弱顺序是HAO4>H2BO4
>H3CO4,则下列判断错误的是
A.非金属性A>B>C B.气态氢化物稳定性HA>H2B>CH3
 C.原子半径A>B>C
D.气态氢化物还原性CH3>H2B>HX
C.原子半径A>B>C
D.气态氢化物还原性CH3>H2B>HX
2.科研人员发现放射性同位素钬。篙舶可有效地治疗肝癌。该同位素原子核内的中子数为
A.99 B.67 C.166 D.233
1.硅被誉为无机非金属材料的主角。下列物品用到硅单质的是
A.陶瓷餐具 B.石英钟表 C.计算机芯片 D.光导纤维
22.(9分)
某同学通过化学反应2H2O2=2H2O+O2下探究催化剂对化学反应速率的影响,设计并完成了下表所示的探究实验:
|
|
实验操作 |
实验现象 |
实验结论 |
|
实验一 |
取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 |
有少量气泡产生,木条不复燃 |
过氧化氢分解产生氧气,但是反应较慢。 |
|
实验二 |
|
|
二氧化锰能加快过氧化氢的分解 |
(1)你认为“实验二”的实验操作应为
实验现象应为
(2)该同学想进一步证明二氧化锰在反应2H2O2=2H2O+O2 中只充当催化剂,又补充设计了两个方面的探究实验:第一方面的实验操作中包含了两次称量,其目的是
中只充当催化剂,又补充设计了两个方面的探究实验:第一方面的实验操作中包含了两次称量,其目的是
; 第二方面的实验利用“实验二”反应后试管内的剩余物继续实验。接下来的实验操作是
现象是
结论为

21.(10分)
下面是某课外活动小组在进行探究乙醇性质实验时遇到的问题,请你帮助解决。
(1)在做乙醇与钠反应的实验时,把一小块钠缓慢放入装有乙醇的试管内,与钠和水反应相比有所不同:钠没有熔化成小球;钠先沉在试管底;反应后逐渐浮起。小组同学进行讨论,前两点现象解释达成共识。请说出你的看法。
钠没有熔化成小球,因为
钠先沉在试管底,因为
第三点现象解释存在争议,活动小组的同学形成两种意见:a生成的氢气产生浮力所致;b生成的乙醇钠增大了溶液的密度所致。请你设计一个实验验证a和b说法的合理性。
(2)在做乙醇的催化氧化实验中,某同学有个意外发现:在酒精灯外焰灼烧铜丝观察到铜丝表面变黑;当铜丝接近灯芯,变黑的铜丝又恢复原来的红色。请用化学方程式解释上述变化过程。
, 。
20.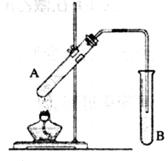 (11分)
(11分)
实验室用右图所示装置制取乙酸乙酯。
(1)A试管中加入碎瓷片的目的是 ;
B试管内盛装的溶液是 ,其作用有 ,
(2)实验前向B试管中加入一滴酚酞试液,实验过程中观察到溶液的红色逐渐变浅,其原因是 。实验中注意长导管不能伸到B试管液面下,原因是
(3)将生成的乙酸乙酯分离出来的实验操作是 ,所需要的主要仪器是
(4)与乙醇和乙酸在浓硫酸催化作用下发生酯化反应相似,某酸和某醇也能发生酯化反应生成酯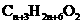 ,若某酸表示为
,若某酸表示为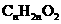 ,则某醇化学式为
,则某醇化学式为
19.(10分)
已知短周期中的5种非金属元素A、B、C、D、E,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零。B原子的最外层电子数是内层电子数的2倍。通常状况下E的单质是黄色晶体,易溶于二硫化碳。D与E在同一主族,C、D在周期表中处于相邻的位置。 .
请回答下列问题:
(1)A元素的名称是 ;E元素的符号是
(2)同时含有A、B、C、D四种元素的一种无机物的化学式是
(3)A的单质和C的单质在一定条件下反应生成化合物X,向X的水溶液中滴入酚酞溶液,可以观察到的现象是 。X在催化剂的作用下与D单质发生反应的化学方程式为
(4)B的单质与E的最高价氧化物的水化物的浓溶液发生反应的化学方程式为
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com