
题目列表(包括答案和解析)
28.(16分)下图中A是H2发生器,B是大小适宜的圆底烧瓶,C是装有干燥剂的U形管,D是装有还原铁粉的反应管。实验前先检查实验装置 的气密性。实验开始时,先关闭活塞W,并取下烧瓶B;向A中加入一定量浓度的盐酸适量,产生H2。经必要的操作后,在导管的出口处点燃氢气,然后如图所示套上烧瓶,塞紧瓶塞,氢气在烧瓶中继续燃烧。用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞W,B瓶中的气体通过U形管后在D中
反应,进入E,最后进入F中(F中装有某种物质的溶液,作检验之用)。
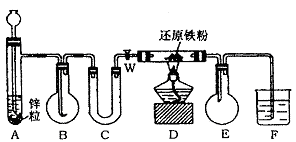
请回答下列问题:
(1)实验前如何检查装置气密性?
__________________________________________________________________________________________________________________________________________________________________________________________________________。
(2)点燃H2前必须进行什么操作?为什么?
__________________________________________________________________________________________________________________________________________________________。
(3)写出B、D中分别发生反应的化学方程式。
B中______________________________________________________。
D中______________________________________________________。
(4)U形管中,应盛试剂是_______________,其作用是____________________。
(5)E装置作用是______________________________。
(6)F中可装_____________的溶液,发生的现象为______________________________。
27.(18分)由于用氯气对饮用水消毒,会使水中的有机物发生氯化,生成有机含氯化合物于人体有害,世界环保联盟即将全面禁止这种消毒方法。建议采用广谱性具有强氧化性的高效消毒剂二氧化氯(ClO2)。ClO2极易爆炸,生产和使用时尽量用惰性气体稀释,避免光照、震动或加热。
(1)在ClO2中,所有原子是否都满足8电子结构?______________(填“是”或“否”)。
(2)欧洲一些国家用NaClO3氧化浓盐酸来制取ClO2,同时有Cl2生成,且Cl2的体积为ClO2的一半。这一反应的化学方程式是___________________________________。
(3)浓盐酸在上述反应中显示出来的性质是_______________(填写编号)。
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
(4)若上述反应产生0.1 mol Cl2,转移电子的物质的量为_______________mol。
(5)ClO2为高效低毒的消毒剂,其消毒的效率(以单位质量得到电子数表示)是Cl2的_____________倍。
(6)我国广泛采用将经干燥空气稀释的氯气通入填有固体亚氯酸钠(NaClO2)的柱内制得ClO2,表示这一反应的化学方程式是_______________________________。和欧洲的方法相比,我国这一方法的主要优点是_______________________________。
26.(12分)双氧水(H2O2)属于“绿色化学”试剂,它具有强氧化性、漂白性和弱酸性。极纯的双氧水很稳定。
(1)某研究性学习小组研究过氧化钠跟水等物质的反应,进行如下实验:向盛有少量过氧化钠固体的试管中滴加水,直至气体不再放出,加入稀释,将所得溶液平均盛放在七支试管中,一支试管中滴加酚酞试液,溶液变红,半分钟内红色褪去;另六支试管中分别加入少量二氧化锰、氧化铜、土豆泥、生锈的铁钉、新鲜动物肝脏或用波长为320~380 nm的光照射后,又有气体放出,待气体放出后,再滴加酚酞,溶液变红,持久不褪色。请写出:
①过氧化钠跟水反应的化学方程式:a._____________;b.____________。
②加入二氧化锰等后溶液中发生反应的化学方程式是________________________,反应中二氧化锰、氧化铜、土豆泥、生锈的铁钉、新鲜动物肝脏的作用是___________________。
③新鲜动物肝脏的提取液稀释10倍与原溶液实验效果基本相同,这表明新鲜肝脏对该反应具有_______________________。
A.专一性 B.多样性 C.高效性 D.稳定性
④研究性学习的结论之一为:“过氧化钠与水反应的还原产物为水,而不是氢氧化钠。”这个结论是否正确?为什么?_________________________________________。
(2)将H2O2溶液滴入含有酚酞的NaOH溶液中,红色消失。甲学生认为这是由于H2O2是二元弱酸,消耗了OH-,而使红色褪去;乙学生认为,H2O2具有强氧化性,将酚酞氧化,红色消失。试设计一个实验论证甲、乙两位学生的解释中哪种正确?
________________________________________________________________________________________________________________________________________________________________________________________________________________。
25.(20分)已知X、Y均为短周期元素,X在空气中燃烧发出耀眼白光。气体G与氢气密度之比为8.5,B是一种化肥的重要组成部分,可由人体 肝脏产生,也可由C分解而成。D是一种高分子化合物,能作为重金属盐中毒后的解毒剂。
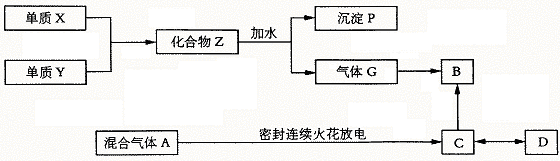 (1)写出X、Y、Z、P、G的化学式。
(1)写出X、Y、Z、P、G的化学式。
(2)写出B、C、D的名称。
(3)A中所含的主要气体成分是______________,这一实验最先由___________________设计完成。
(4)C分解成B是通过____________________作用。D是生物体内的_________________细胞器合成。
(5)Z与水的反应方程式是_____________________,并计算生成1 mol气体G时应同时得到_____________mol沉淀P。
23.(17分)下面示光合作用的实验过程:
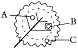 ①选一株银边天竺葵,预先放在阴暗处两昼夜,再用2 cm×2 cm不透光的黑纸用大头针别在这株天竺葵叶片的绿色部位(如右图),然后将其放在阳光下照射6~8小时,剪下该叶片,并用瓶塞穿孔器分别在叶片的不同部位取A、B、C三个圆叶片(B为遮光处取下的圆片,C为银边处取下的圆片)
①选一株银边天竺葵,预先放在阴暗处两昼夜,再用2 cm×2 cm不透光的黑纸用大头针别在这株天竺葵叶片的绿色部位(如右图),然后将其放在阳光下照射6~8小时,剪下该叶片,并用瓶塞穿孔器分别在叶片的不同部位取A、B、C三个圆叶片(B为遮光处取下的圆片,C为银边处取下的圆片)
②将3个叶圆片放在装有酒精的试管里经热水浴脱色,并将它们放在清水中漂洗。
③再将经过漂洗的叶圆片放在白纸上,然后用吸管吸取碘液,分别滴在三个叶圆片上
请分析回答:
(1)将天竺葵预先放在阴暗处两昼夜的目的是_____________________________。
(2)将叶片放在装有酒精的试管里经热水浴脱色是为了____________________________。
(3)分析A、B、C三个叶圆片的颜色反应的情况:
A:__________________________________________________________________;
B:__________________________________________________________________;
C:__________________________________________________________________。
(4)把叶圆片A切成薄片制成装片放在显微镜下观察,发现细胞中分散着被染成蓝色结构的是_____________,光合作用的产物淀粉是在_____________________________阶段形成的。
(5)该实验证明光合作用的必需条件是__________________________________,场所是_____________________________________。
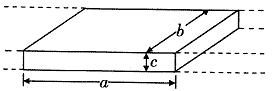
22.电磁流量计广泛应用于测量可导电流体(如污水)在管中的流量(在单位时间内通过管内横截面的流体的体积)。为了简化,假设流量计是如图所示的横截面为长方形的一段管道,其中空部分的长、宽、高分别为图中的a、b、c。流量计的两端与输送流体的管道相连接(图中虚线),图中流量计的上下两面是金属材料,前后两面是绝缘材料,现于流量计所在处加磁感应强度为B的匀强磁场,磁场方向垂直于前后两面,当导电流体稳定地流经流量计时,在管外将流量计上、下两表面分别与一串接了电阻R的电流表的两端连接,I表示测得的电流值,已知流体的电阻率为ρ,不计电流表的内阻,则可求得流量为
A.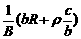
B.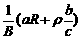
C.
D.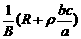
第Ⅱ卷(非选择题 共168分)
21.如图所示,a、b、c是一条电场线的三点,电场线方向由a到c,ab间距离等于bc间距离,用Φa、Φb、Φc和Ea、Eb、Ec分别表示a、b、c三点的电势和场强可以判定
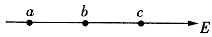
A.Φa>Φb>Φc
B.Ea>Eb>Ec
C.Φa-Φb=Φc-Φd
D.Ea=Eb=Ec
20.如图为一理想变压器,原线圈匝数为n1=1000匝,副线圈匝数n2=100匝,电阻R=10 Ω。原线圈中接有220 V的正弦式电流,电压表和电流表均为理想电表,则电压表和电流表读数分别是

A. 22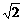 V,2.2
V,2.2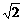 A
A
B.22 V,2.2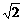 A
A
C.22 V,2.2 A
D.22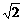 V,2.2 A
V,2.2 A
19.一只玩具电动机用一节干电池供电,闭合开关后发现电机转速较慢,经检测电动机性能完好,S闭合时用电压表测ab间电压只有0.6 V,断开开关S,测得ab间电压接近1.5 V,则电动机转速慢的原因是
A.开关S接触不良
B.电动机两端导线接触不良
C.电动机两端接线短路
D.电池过旧,内阻过大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com