
题目列表(包括答案和解析)
4. 细菌的细胞质中有哪些结构?
3. 细菌的核区内的液体控制细菌的主要遗传性状吗?
2. 细菌的细胞壁与植物细胞壁成分相同吗?
1. 细菌是单细胞原核生物吗?
33.(12分)(1)如图所示是利用高频交流电焊接自行车零件的原理示意图,其中外圈A是通高频交流电的线圈,B是自行车的零件,a是待焊接的接口,接口两端接触在一起。
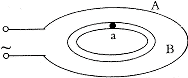
当A中通有交变电流时,B中会产生感应电流,便使接口处金属熔化而焊接起来。为什么在其他条件不变的情况下,交变电流的频率越高,焊接越快?
(2)分析为什么焊接过程中,接口a处已被熔化而零件的其他部分并不很热?
(3)NH4Cl常用在金属焊接上,以除去金属表面上的氧化物薄层,请用方程式表示除锈的过程。
(4)高频焊接时线圈中通过高频交流电,金属工件的焊缝中就产生大量焦耳热,要使焊接处产生的热量较大,可采用
A.增大交变电流的电压
B.增大交变电流的频率
C.增大焊接缝的接触电阻
D.减少焊接缝的接触电阻
32.(17分)如图所示,一个带电小物块P,沿一个绝缘的倾斜轨道向上运动,设运动过程中P的带电量保持不变,空间存在着匀强电场(未在图中画出)。
已知P经过A点时动能30 J,经过B点时动能减少了10 J,机械能增加了20 J,电势能减少了35 J,P运动到C点时速度刚好减为零。(设小物块P所受滑动摩擦力的大小不变)
(1)求小物块P从A到C的运动过程中,克服摩擦力所做的功。
(2)小物块P到达C点后会不会沿轨道向下运动?为什么?
31.(12分)对宇宙的分析研究中,一个最有趣的宇宙物体就是所谓的“黑洞”,它是某些类型星体(设质量为M的均匀球)的最后演变期。研究证明,黑洞确实存在,设星体表面发出频率为ν的光子,其能量为hν,由爱因斯坦质能方程,光子的质量可以描述为m=hν/c2;已知质量为m的粒子,离星体中心为r0处的引力势能为Ep=-GMm/r0,此处h为普朗克常数,c为光速,G为万有引力恒量。根据黑洞的性质,我们可以用能量守恒原理近似地求解黑洞临界半径R的数量级。
(1)简述“黑洞”最主要的一个物理性质。
(2)试求解黑洞临界半径R。
 (3)据分析,太阳演变的最后阶段,很可能变成所谓的“黑洞”,如已知太阳的质量为6×1030 kg,估算太阳变成黑洞时的半径R。
(3)据分析,太阳演变的最后阶段,很可能变成所谓的“黑洞”,如已知太阳的质量为6×1030 kg,估算太阳变成黑洞时的半径R。
30.(16分)(1)在“测定金属的电阻率”的实验中,电阻丝的电阻约为4-6 Ω?,可供选择的主要器材如下:
A.电压表(量程0-3 V,内阻15 kΩ)B.电流表(量程0-0.6 A,内阻2 Ω)
C.电流表(量程0-1 A,内阻0.5 Ω)D.滑动变阻器(额定电流1 A,内阻20 Ω)
E.滑动变阻器(额定电流0.5 A,阻值为1 000 Ω)
F.电池组(电动势为4 V,内阻为0.5 Ω)
要求测量时误差小,电压从0开始调节,滑动变阻器向左滑动时电压变大。
①电流表应选___________,滑动变阻器应选___________。
②把下图所示的器件,连接成测量电路。
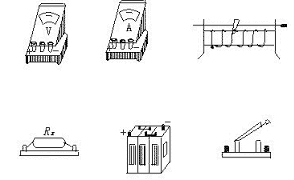
(2)如图为一个理想变压器的示意图,输出端有两组线圈。现在三个小灯泡L1:“6 V、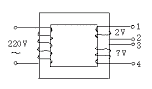 0.9 W”,L2:“6 V、0.9 W”,L3:“3 V、0.9 W”。要使它们接在同一电路上都能正常发光,在答题纸上画出它们的接线图,这时初级线圈中电流的最大值Im=___________A。
0.9 W”,L2:“6 V、0.9 W”,L3:“3 V、0.9 W”。要使它们接在同一电路上都能正常发光,在答题纸上画出它们的接线图,这时初级线圈中电流的最大值Im=___________A。
29.(24分)某工厂废液经测定得知主要含有乙醇,其中还溶有丙醇、乙酸和乙酸乙酯。现欲从废液中回收乙醇和乙酸,根据各物质的沸点,补充下列实验步骤,模拟实现这一过程,并回答有关问题。
|
物质 |
丙酮 |
乙酸乙酯 |
乙醇 |
乙酸 |
|
沸点/℃ |
56.2 |
77.06 |
78 |
117.9 |
可供选择的实验用品:
1 mol·L-1烧碱溶液;18.4 mol·L-1硫酸;蒸馏水和冰;400 mL烧杯;250 mL烧杯;
250 mL蒸馏烧瓶;温度计;冷凝器;接受器;玻璃棒以及中学化学实验的常用仪器。
(1)补充下列实验步骤:
①组装蒸馏装置,检查气密性;
②取100 mL废液注入250 mL蒸馏烧瓶中,滴入1 mol·L-1烧碱溶液,调废液pH=10;
③___________; ④___________;
⑤___________; ⑥___________。
(2)滴入1 mol·L-1烧碱溶液,使溶液的pH=10的目的是___________。
(3)用18.4 mol·L-1硫酸的目的是(用化学方程式表示):___________。
(4)最后蒸馏烧瓶内残留液中的溶质的主要成分是___________。
28.(18分)碘缺乏症遍及全球,多发生于山区,南美的安第斯山区、欧洲的阿尔卑斯山区和亚洲的喜马拉雅山区是高发病地区。我国云南、河南等10余省的山区发病率也较高。据估计我国患者大约有100万人。为控制该病的发生,较为有效的方法是食用含碘食盐。我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3)。据此回答下列问题:
(1)碘是合成下列哪种激素的主要原料之一
A.胰岛素 B.甲状腺激素 C.生长激素 D.雄性激素
(2)长期生活在缺碘山区,又得不到碘盐的供应,易患
A.甲状腺亢进 B.佝偻病 C.地方性甲状腺肿 D.糖尿病
(3)可用盐酸酸化的碘化钾和淀粉检验食盐中的碘酸钾。反应的化学方程式为___________,氧化产物与还原产物的物质的量之比为___________,能观察到的明显现象是___________。
(4)已知KIO3可用电解方法制得。原理是:以石墨为阳极,以不锈钢为阴极,在一定电流强度和温度下电解KI溶液。总反应化学方程式为:KI+3H2O======KIO3+3H2↑,则两极反应式分别为:阳极___________,阴极___________。
(5)在某温度下,若以12 A的电流强度电解KI溶液10 min,理论上可得到标况下氢气___________L。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com