
题目列表(包括答案和解析)
2.下表是几种碳酸盐的分解温度和阳离子半径
|
碳酸盐 |
MgCO3 |
CaCO3 |
SrCO3 |
BaCO3 |
|
热分解温度/℃ |
402 |
900 |
1172 |
1360 |
|
阳离子半径/pm |
66 |
99 |
112 |
135 |
分析上表可以得出
A.离子晶体中阳离子的半径越大,越易分解
B.离子晶体中阳离子的半径越小,越易分解
C.离子晶体中阳离子的半径越大,结合碳酸根中的氧离子越容易
D.离子晶体中阳离子的半径越小,结合碳酸根中的氧离子越容易
1.离子晶体之间的决定于离子键的大小,下列按离子键由大到小排列的是
A.NaF>NaCl>NaBr>NaI B.Na2O >Na2S>NaCl>NaI
C.NaCl>CaCl2>MgCl2>AlCl3 D.MgCO3> CaCO3> SrCO3> BaCO3
3.2《离子键》
21.(8分)标准状况下,用一定量的水吸收氨气后制得浓度为12.0 mol·L-1、密度为0.915 g·cm-3的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。
(本题中氨的式量以 17.0计,氨水的溶质以溶解的NH3为准,水的密度以1.00g·cm-3计)
20.(8分)现用Zn与实验室中的盐酸反应制取4.48L H2(标准状况)。
(1)如果选用所贴标签为2.0mol·L-1的盐酸,至少需该盐酸多少毫升?
 (2)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升?
(2)如果选用所贴标签为7%(密度为1.043g·mL-1)的盐酸,至少需该盐酸多少毫升?
18(10分).有人设计了如图所示实验装置,目的是做钠与水反应实验,并验证①钠的物理性质;②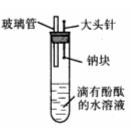 钠与水反应的产物是什么。
⑴当进行适当操作时还需要的仪器有 。
⑵如何进行操作? 。
⑶实验现象是 。
钠与水反应的产物是什么。
⑴当进行适当操作时还需要的仪器有 。
⑵如何进行操作? 。
⑶实验现象是 。
19.(13分)下图为配制0.2mol·L-1Na2CO3溶液250mL示意图。

回答下列问题:
(1)①中称得Na2CO3_____________g。
(2)玻璃棒在②、③两步中的作用分别是_____________、_____________。
(3)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.某同学在第⑧步观察液面时俯视_____________;
B.没有进行操作步骤④和⑤_____________;
C.在第⑤步不慎有少量液体流到容量瓶外_____________。
17.(10分)现有X、Y、Z三种元素。
 (1)X的单质可以在Z的单质中燃烧生成XZ,火焰为苍白色。
(1)X的单质可以在Z的单质中燃烧生成XZ,火焰为苍白色。
(2)XZ极易溶于水,其水溶液可使蓝色石蕊试纸变红。
(3)X、Y、Z的单质在常温下为气体。
(4)两分子X的单质可以和Y单质化合生成两分子X2Y(常温下为液体)。
(5)Z的单质溶于X2Y中得到溶液具有漂白性,推断
①XYZ各为何元素(写元素符号)?X__________ Y__________ Z__________
②XZ和X2Y各是什么物质(写化学式)? XZ__________ X2Y__________
16.(6分)100mlA2气体跟50mlB2气体恰好完全反应,生成的气体体积为100ml(同温同压条件下),试推断气体生成物的化学式__________,推断的依据是__________________________。
15.在一定温度、压强下,1体积X2(气)和3体积Y2(气)化合生成2体积的气体化合物,则该气体化合物的化学式为( )
A.XY3 B.XY C.X3Y D.X2Y3
第Ⅱ卷(非选择题 共55分)
14.在标准状况下,相同质量的下列气体,占有体积由大到小的顺序是( )
① Cl2 ② H2 ③ N2 ④ CO2 ⑤ O2
A.③ ② ④ ⑤ ① B.③ ② ④ ③ ①
C.① ④ ⑤ ② ③ D.② ③ ⑤ ④ ①
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com