
题目列表(包括答案和解析)
5.在物质分类中,前者包括后者的是 ( )
A.氧化物、化合物 B.化合物、电解质
C.溶液、 胶体 D.溶液、 分散系
4. 下列实验操作中错误的是 ( )
A.在由氢氧化铜分解制氧化铜时,要边加热边用玻璃棒搅拌
B.用药匙或者纸槽把粉末状药品送入试管的底部
C.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 D.刚完成蒸发结晶,因要做下一个实验,可以将蒸发皿先放在桌面上,冷却后收好。
3.设NA表示阿伏加德罗常数,则下列说法中正确的是( )
A.含Fe(OH)3为1mol的氢氧化铁胶体分散系中,分散质的粒子个数为NA
B.0.5mol 钠与氯气发生反应转移的电子数为NA
C.同温同压下,分子数相同的氧气和氮气所占体积也一定相同
D.在标准状况下,4.48L CCl4中所含的原子总数为NA
2.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域做出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是 ( )
A.化学不做实验就什么都不知道 B.化学不再需要实验
C.化学不再是纯实验科学 D.未来化学的方向是经验化
1.人们对于化学科学有各种各样的认识,其中错误的是 ( )
A.化学面对改善人们生活显得生机勃勃,面对自然环境的日益恶化无能为力
B.化学是一门以实验为基础的自然科学,可以培养学生动手能力
C.化学是一门具有极强实用性的科学,应该予以重视
D.化学将在能源、资源的合理开发和安全应用方面大显身手
22、(6分)在20℃时,将3.16gKNO3溶于10g水中,恰好配成密度为1.13g/cm3的饱和溶液.试求:
(1)此饱和溶液中KNO3的质量分数。
(2)此饱和溶液中KNO3的物质的量浓度。
21、(6分)将250mLH2SO4的质量分数为98%,密度为1.84g/cm3的浓硫酸稀释到1000mL。
(1)此时溶液中H2SO4的物质的量是多少?
(2)此时溶液中H+的物质的量浓度是多少?
20、(14分)用18mol/L 浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④检漏、 转移、洗涤 ⑤ 定容、摇匀
回答下列问题
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是
(从下列中选用 A. 10ml B. 25ml C. 50ml D. 100ml)
(2)第③步实验的操作是
(3)第⑤步实验的操作是
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A. 所用的浓硫酸长时间放置在密封不好的容器中
B. 容量瓶用蒸馏水洗涤后残留有少量的水
C. 所用过的烧杯、玻璃棒未洗涤
D. 定容时俯视溶液的凹液面
19、(12分)为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
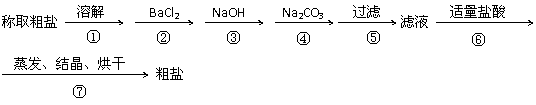 (1)判断BaCl2已过量的方法是
(1)判断BaCl2已过量的方法是
。
(2)第④步中,写出相应的离子方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
 。
。
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
。
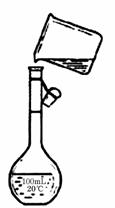
(4)为检验精盐纯度,需配制250 mL 0.2 mol/L NaCl(精盐)溶液,题图是该同学转移溶液的示意图,图中的错误是
。
18、(10分)有一包白色固体,可能含有Na2CO3,Na2SO4,KNO3,CuSO4,BaCl2中的若干种,现用它做以下实验,并得到相应现象:
(1)取少量固体粉末加到足量水中,得到白色悬浊液,静置后下部为白色沉淀,上层为无色澄清溶液。
(2)若取(1)中的沉淀,加入足量稀硝酸,白色沉淀消失,并有气泡产生。
根据上述实验现象判断。该白色固体中一定有 ,一定不会有 ,可能会有 ;上述实验中有关反应的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com