
题目列表(包括答案和解析)
以下1-15题每小题2分,共30分,每小题只有一个正确答案)
1. 科学家在2000年8月10日出版的英国《自然》杂志上报告,他们用DNA制造出了一种臂长只有7纳米的纳米级粒子,以便能够钳起分子或原子并对它们随意组合。下列分散系中的分散质的粒子直径与纳米粒子具有相同数量级的是
A.溶液 B.胶体 C.悬浊液 D.乳浊液
20. (13分)科学探究:
某学习小组根据图中所示的电解水原理进行实验,并对实验得到的与查阅资料获得的数据进行处理、分析,请与他们一起进行探究。请按要求填写。
(1)观察不同时间试管内的H2和O2体积的比值均约为 。
(2)假设电解了1.8g H2O,根据电解水的化学方程式计算生成H2、O2的质量,计算过程如下:
并填表如下:
|
|
质量g |
物质的量mol |
H2 和O2物质的量的比 |
|
H2 |
|
|
|
|
O2 |
|
|
根据(1)的实验观察与推算初步得到的一个结论是:在相同的温度和压强下,
(3)下表列出了一些物质的密度,请计算出1 mol这几种物质的体积。
|
条件 |
物质 |
密度/g·cm-1 |
1 mol物质的体积 |
|
0℃101kPa |
H2 |
0.0899 |
|
|
O2 |
1.43 |
22.4
L |
|
|
CO2 |
1.96 |
22.4 L |
|
|
20℃ |
Fe |
7.86 |
7.12 mL |
|
Al |
2.70 |
|
|
|
H2O |
0.998 |
|
|
|
H2SO4 |
1.83 |
53.6 mL |
根据上表数据,得出的结论是(至少写出三点)
(1)在相同的温度压强下,
(2)
(3)
(4)
19. (5分)现有体积为200mL,质量为0.270kg,质量分数为10%的CuCl2溶液。请计算:(1)溶液中CuCl2的物质的量是多少?
(2)溶液Cu2+、Cl-物质的量是多少?
 (3)溶液Cu2+、Cl-物质的量浓度各是多少?
(3)溶液Cu2+、Cl-物质的量浓度各是多少?
18. (14分)已知五种白色粉末分别是KNO3、Na2CO3、MgCl2、Ba(OH)2、CuSO4中的一种。现提供蒸馏水与盐酸两种试剂,对这些物质进行鉴别(被鉴别出的物质可作为试剂来鉴别其他物质)。某学习小组按着以下步骤进行鉴别,请填写下列表格,并回答问题(物质请用化学式表示,其余按要求填写):
步骤1:分别取五种白色粉末少量于五个小烧杯(已编号)中,加入蒸馏水,搅拌,得到五种溶液。 (五种溶液没有倒掉,待下面的实验再取用。)
|
加入试剂 |
被检出物质 |
被检出物质发生电离的 电离方程式 |
|
H2O |
|
|
步骤2:分别取其余的四种溶液少量于四支小试管,分别滴加盐酸。
|
加入试剂 |
被检出物质 |
离子方程式 |
|
HCl |
|
|
|
有反应,但没有明显现象而暂时未被检出物质 |
离子方程式 |
|
|
|
|
步骤3:分别另取其余的三种溶液少量于三支小试管,分别滴加CuSO4溶液。
|
加入试剂 |
被检出物质 |
离子方程式 |
|
CuSO4 |
|
|
步骤4:分别另取其余的二种溶液少量于二支小试管,分别滴加已经被鉴别出物质的溶液,根据是否有变化现象的从而鉴别其余两种物质。
|
加入试剂 |
被检出物质 |
离子方程式 |
|
|
|
|
判断推导:
(1)实验过程中发生的反应根据不同的分类标准,它们均属于 (填序号)
①离子反应 ②非离子反应 ③氧化还原反应 ④复分解反应
⑤分解反应 ⑥化合反应 ⑦置换反应
(2)它们所属反应类型发生反应的条件是: 、
或 。只要具备上述条件之一,反应就能发生。
17. (8分)蒸馏是实验室制备蒸馏水的常用方法。
⑴图I是实验室制取蒸馏水的常用装置,
图中明显的一个错误是 。
⑵仪器A的名称是 ,仪器B的名称是 。
⑶实验时A中除加入少量自来水外,还需加入几粒 ,其作用是防止液体暴沸。
 ⑷从锥形瓶取少量收集到的液体于试管中,然后滴入
⑷从锥形瓶取少量收集到的液体于试管中,然后滴入
和 (填试剂的化学式),检验是否存在Cl-。
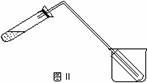
(5)图II装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图I完全相同。该装置中使用的玻璃导管较长,其作用是 ;烧杯中最好盛有的物质是 (填名称)。
16. 工业上制取ClO2的化学反应:2NaClO3 + SO2 + H2SO4 = 2ClO2 + 2NaHSO4,下列说法正确的是 ( )
A. NaClO3在反应中化合价降低,失去电子
B. SO2在反应中发生氧化反应
C. 2mol氧化剂在反应中得到2mol电子
D. H2SO4 在反应中作氧化剂
 第二部分非选择题(共40分)
第二部分非选择题(共40分)
15. 下列化学变化中,需加入还原剂才能实现的是 ( )
A.CuO→CuCl2 B.CuO→Cu C.CO→ CO2 D.H+→H2
14. 能正确表示下列化学反应的离子方程式的是 ( )
A.CuSO4溶液中加入铁粉: Fe + Cu2+ = Cu + Fe2+
B.铁与稀硫酸反应: 2Fe + 6H+ = 2Fe3+ + 3H2↑
C.氢氧化钡溶液与硫酸反应: Ba2++OH-+H+ +SO42-= BaSO4+H2O
D.澄清石灰水中通人少量二氧化碳: Ca 2++2OH- + CO2 = CaCO3↓+H2O
13. 下列分类标准正确的是 ( )
A.化学反应分为:离子反应、非离子反应(标准:是否在水溶液中进行)
B.分散系分为:溶液、胶体、浊液(标准:能否透过滤纸)
C.化学反应分为:氧化还原反应、非氧化还原反应(标准:元素化合价是否发生变化)
D.化合物分为:电解质、非电解质(标准:溶于水或熔融状态能否导电)
12. 关于胶体和溶液的区别,下列叙述中正确的是 ( )
A.FeCl3溶液与Fe(OH)3胶体的外观都是澄清、透明、均匀的
B.溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
C.光束通过稀豆浆时,可以看到一条光亮的“通路”,光束通过蔗糖溶液时,则看不到一条光亮的“通路”
D.溶液最稳定,放置后不会生成沉淀;胶体很不稳定,放置后很快会生成沉淀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com