
题目列表(包括答案和解析)
2.下列说法不正确的是
A. 磷酸的摩尔质量与6.02×1023个磷酸分子的质量在数值上相等
B. 6.02×1023氮分子和6.02×1023个氢分子的质量比是14︰1
C. 32g氧气所含的原子数目约为2×6.02×1023
D. 常温常压下,0.5×6.02×1023个一氧化碳分子所占的体积约为11.2L
1.下列实验中均需要用到的仪器是
1配制一定物质的量浓度的溶液 2过滤 3蒸发 4pH试纸的使用
A. 试管 B. 容量瓶
C. 玻璃棒 D. 漏斗
27.(6分)(1)16g (2) 20mL (3) 25g (每3*4=12分)
26.(18分)(1)
|
分类标准 |
金属单质 |
氧化物 |
溶液 |
胶体 |
电解质 |
|
属于该类的物质 |
② |
③④ |
⑧ ⑨ |
⑦ |
③⑤⑥⑩ |
(2)Ba(OH)2+2HNO3=Ba(NO3)2+2H2O

(3)Al2(SO4)3= 2Al3++3SO42-, 9.03×1022, 0.6mol/L。
(4)Ba2++2OH-+CO2=BaCO3↓+H2O。
(5)HNO3,1︰1,0.6mol。 Al+4H++NO3-=Al3++NO↑+2H2O
25.(14分)(1)取第②步后的上层清液1-2滴于点滴板上(或取少量上层清液于试管中),再滴入1-2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(4分)(合理答案皆可)
(2)Ca2+ + CO32- = CaCO3↓; Ba2+ + CO32- = BaCO3↓
(3)NaOH 过滤 (2*2=4分)
(4)否;过量的BaCl2必须要用Na2CO3除去,步骤复杂; 是 ;(2*3=6分)
(5)会有部分沉淀溶解,从而影响制得精盐的纯度(2分)
24.(8分)(1)蒸馏烧瓶;冷凝管;容量瓶(各2*3=6分)
(2)④(2分)(3)温度计;(2分)分馏;(2分)
未用玻璃棒引流;(2分)未采用250ml容量瓶(各2分)
23.(10分) 49
3.01×1023 2 1 36.5
 .
.
1.B. 2. B. 3. D. 4. C. 5. C.6. C. 7.B. 8. D. 9. B. 10. D. 11. C. 12.C. 13.D 14. B. 15. A. 16. D. 17. D.18. A.19. B.20.A.21.D.22. D.
第Ⅱ卷 (共56分)
27.(6分)现欲配制100 mL 1.0 mol/L的硫酸铜(CuSO4)溶液,试求:
(1)若用无水硫酸铜配制,则需要无水硫酸铜粉末的质量是多少?
(2)若用5.0 mol/L CuSO4溶液配制,则需要该溶液多少毫升?
(3)若用胆矾(CuSO4 5H2O)配制,则需要胆矾的质量是多少?
高一上学期期中考试
26.(18分)现有下列十种物质:①H2 ②铝 ③CuO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)按物质的分类方法填写表格的空白处: 

|
分类标准 |
|
氧化物 |
|
|
电解质 |
|
属于该类的物质 |
② |
|
⑧ ⑨ |
⑦ |
|
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-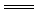 H2O,该离子反应对应的化学方程式为
。
H2O,该离子反应对应的化学方程式为
。
(3)⑩在水中的电离方程式为 ,17.1g⑩溶于水配成250mL溶液,SO42-的粒子数为 ,SO42-的物质的量浓度为 。
(4)少量的④通入⑥的溶液中反应的离子方程式为 。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3 = Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是 (填化学式),还原剂与氧化剂的物质的量之比是 ,当有5.4g Al发生反应时,转移电子的物质的量为 。
该反应的离子方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com