
题目列表(包括答案和解析)
6.下列物质中所含分子数最多的是
A.56g N2 B.1.5 mol O2
C.100g Cl2 D.3.01×1023个SO2分子
5.下列说法不正确的是
A.物质的量是可以把物质的质量与微观粒子数联系起来的一个基本物理量
B.摩尔是国际单位制中七个基本物理量之一
C.1mol任何微观粒子的质量以克为单位,数值上等于该粒子的相对原子(分子)质量
D.含有6.02×1023个粒子的任何微观粒子集体计量为1摩尔
4.溶液、胶体和浊液这三种分散系的根本区别是
A.是否是大量分子或离子的集合体 B.是否能通过滤纸
C.分散质粒子直径的大小 D.是否均一、透明、稳定
3.欲萃取碘水中的I2 ,不能作为萃取剂的是
A.酒精 B.苯
C.CCl4 D.汽油
2.下列叙述正确的是 ( )
A.1 mol H2O的质量为18g·mol-1
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4L
1.下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )


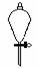

A. 蒸馏、蒸发、萃取、过滤 B. 蒸馏、过滤、萃取、蒸发
C. 萃取、过滤、蒸馏、蒸发 D. 过滤、蒸发、萃取、蒸馏
25. 取1.06g Na2CO3,溶于水配成10 mL溶液,再往该溶液滴入足量稀盐酸至完全反应。
求:(1)写出相关离子方程式
(2)该Na2CO3溶液的物质的量浓度?
(3)标准状况下,生成气体的体积?

24.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.苯取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1) 分离饱和食盐水与沙子的混合物。
(2) 从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3) 分离水和汽油的混合物。
(4) 分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)、的混合物。
23.用98%的浓H2SO4( =1.84g/cm3)配制500ml 0.5mo1/L的稀H2SO4,请按要求填空:
=1.84g/cm3)配制500ml 0.5mo1/L的稀H2SO4,请按要求填空:
(1)所需浓H2SO4的体积为
(2)如果实验室有10mL、20 mL、50mL量筒,应选用 mL量筒,实验中还需要用到的仪器有
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷至室温即进行定容
②定容时俯视刻度线
(4)若定容时液面高于刻度线应采取的措施是
22.(1)lmol H2SO4中含 mol硫原子, 个氧原子。
(2)4.5g水与 g硫酸所含的分子数相等,它们所含氧原子数之比是 ,氢原子数之比是 。
(3)下列物质能导电的是 ,属于电解质的是 ,属于非电解质的是 。
①水银 ②烧碱 ③大理石 ④氯化钠晶体 ⑤盐酸 ⑥干冰 ⑦蔗糖
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com