
题目列表(包括答案和解析)
23.Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4 + 6Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,对此反应下列说法中正确的是
A.Na2O2在反应中只作氧化剂 B.Na2FeO4既是氧化产物又是还原产物
C.O2是还原产物 D.2mol FeSO4发生反应时,反应中共有8mol电子转移
22.为了确定某物质是否变质,所选试剂(括号内物质)达不到实验要求的是:
A.K2SO3是否被氧化(BaCl2) B.新制氯水已经完全变质(品红试液)
C.KI是否被氧化(淀粉溶液) D.漂白粉是否变质(盐酸)
21.下列关于碳酸钠和碳酸氢钠的比较中,正确的是:
A.相同温度下,在水中,碳酸氢钠的溶解度大于碳酸钠的溶解度
B.碳酸钠的热稳定性大于碳酸氢钠的热稳定性
C.相同物质的量的两种固体分别与100 mL 0.100 mol/mol盐酸反应,放出二氧化碳气体是碳酸氢钠多,反应速率是碳酸氢钠的大
D.二者水溶液都显碱性,但物质的量浓度相同时,碳酸氢钠溶液的pH大于碳酸钠溶液的pH
20.下列反应的离子方程式正确的是
A.过量二氧化碳通入偏铝酸钠溶液中:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32-
B.用氢氧化钡溶液中和硫酸溶液:Ba2++SO42-=BaSO4↓
C.氯化铝溶液中加入过量氨水:Al3++3NH3·H2O==Al(OH)3↓+3NH4+
D.醋酸与氢氧化钠溶液:H++OH-==H2O
19.能与铝反应产生氢气的溶液中,一定能大量共存的离子组是
A.NH4+、Cu2+、Cl-、NO3- B.K+、Na+、SO32-、S2-
C.K+、Na+、AlO2-、SO42- D.Ba2+、Na+、Cl-、Br--
18.下列说法正确的是
A.9g水和标准状况下11.2LH2O所含分子数相同
B.同温同压下,氦气的体积是氢气的两倍,则氦原子数与氢原子数之比为2:1
C.同温同压,相同质量的CO和N2具有相同体积。
D.不同气体若体积不同,它们所含分子数也不同
17.下列提纯方法不正确的是
A.除去KNO3中的NaCl杂质----结晶、重结晶 B.除去食盐中的泥沙--------过滤
C.除去KCl中的K2CO3----加适量盐酸 D.除去碘水中的水--------升华
16.亚硝酸(HNO2)参加反应时,既可作氧化剂,也可作还原剂。当它作还原剂时,可能生成的产物是 A.NH3 B.N2 C.N2O3 D.HNO3
14.下列变化过程中不能直接实现的是 ①HCl ②Cl2 ③Ca(ClO)2 ④HClO ⑤CO2
A.①→② B.②→③ C.③→④ D.④→⑤
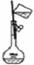 15
15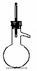

 .下列仪器常用于物质分离的是
.下列仪器常用于物质分离的是

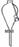
 ① ② ③ ④ ⑤
⑥
⑦
① ② ③ ④ ⑤
⑥
⑦
A.③⑤⑦ B.②③⑤ C.②⑤⑦ D.①②⑥
13.a gH2O中含有b个氢原子,则阿伏加德罗常数为
A.b/amol-1 B.9b/a mol-1 C.18b/a mol-1 D.36b/a mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com