
题目列表(包括答案和解析)
2.含相同分子数的H2O和NH3一定具有相同的( )
A. 物质的量 B. 原子个数 C. 质量 D. 体积
1.除去铜粉中混的有少量氧化铜,其主要操作过程是( )
A.在空气中燃烧 B.加适量稀硫酸、微热、过滤
C.加适量水、微热、过滤 D.加适量稀硫酸、微热、蒸发
20.(8分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物,“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补贴药物,该药品不溶于水但能溶于人体中的胃酸
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
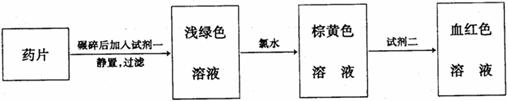
(1)试剂二是____________________________
(2)加入新制氯水后溶液中发生的离子反应方程式是______________________________
___________________________;
(3)加入试剂二后溶液中颜色由棕黄色转变为血红色的是因为_____________________
___________________________________________________________________________
(4)若向FeCl2溶液中加入NaOH溶液,可以发现生成沉淀,而且沉淀暴露在空气中将有颜色变化,此颜色变化为__________________________________________________
__________________________________________________________________________。

19.(24分)禽流感病毒是一种没有超常抵抗力的病毒,研究证明,许多常用消毒药物如84
消毒液、漂粉精、漂白粉、高锰酸钾等,可以将禽流感病毒杀灭,某同学查阅相关资料
并想利用氢氧化钠溶液中通入氯气的方法来制备84消毒液。
(1)(6分)某同学拟采用在氢氧化钠溶液中通入氯气的方法来制备84消毒液,写出该过程的离子方程式______________________________。
84消毒液目前在家庭和公共场合应用广泛,在其发挥重要作用时必然要先发生的化学方程式为____________________________________。为增强器消毒效率,有时采用稀盐酸酸化的方法,用离子方程式来描述其作用原理______________________________。
(2)(8分)该同学首先配制0.5mol/L的NaOH溶液500mL,回答有关问题:
①在实验过程中除玻璃棒、量筒、胶头滴管、试剂瓶外,还需的主要仪器有________、_____________________和_______________________。
②下列操作会使配溶液浓度偏低的是______________(填选项代号)
A.用天平称量氢氧化钠固体时,发现固体稍有潮解现象
B.容量瓶中有少量的蒸馏水
C.没有将洗涤烧杯和玻璃棒的溶液加入容量瓶中
D.定容时有些蒸馏水落到容量瓶外
E.定容读数时,仰实容量瓶的刻度线
F.定容腰匀后发现容量瓶中液面低于刻度线,又加水
(3)(10分)为了制备氯气,该生查阅资料发现实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:
 (浓)
(浓)
 易溶于水)
易溶于水)
①请用双线桥法对该反应进行标注_____________________________________________
_________________________________________________________________________
②写出该反应的离子方程式___________________________________________________
_________________________________________________________________________
③该生为其配制的500mL0.5mol/L氢氧化钠溶液用完,要制备标况下的氯气的体积最少为_____________L,反应中转移的电子的物质的量为___________mol,反应中被氧化的HCl的物质的量为____________mol。
18.(12分)氧化铜是一种黑色固体,可溶于稀硫酸、某同学想知道是稀硫酸的哪种粒子(H2O,H+,SO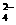 )都使氧化铜溶解,请你和他一切通过如图I、II和III三个实验完成这次探究活动
)都使氧化铜溶解,请你和他一切通过如图I、II和III三个实验完成这次探究活动
(1)提出假设:假设1:H2O能使氧化铜溶解
假设2:__________________
假设3: 能使氧化铜溶解
能使氧化铜溶解
(2)通过实验I可以证明假设_______(填1、2、3)不成立;
(3)要证明另外两种粒子能否溶解氧化铜,还需要进行实验II和III,在II中加入稀硫酸后氧化铜溶解,则进一步所做的实验操作是:在III中先加入___________________,再加入_________________。
(4)探究结果为______________________(用离子方程式表示)你认为除实验II和III所用的试剂外,也反映着一探究结果的能溶解氧化铜的一种常见物质是______________。
17.(8分)现有m g 某气体,它由双原子分子构成,它的摩尔质量为Mg ·mol-1,若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________________mol。
(2)该气体所含原子总数为______________个。
(3)该气体在标准状况下的体积为_________L。
(4)该气体溶于1L水中(不考虑反应),所得溶液的密度为1.5g/mL,其溶液的物质的量浓度为__________________mol/L。
2、答题前将密封线内的项目填写清楚。
16.已知Br元素的最低化合价是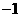 价,最高化合价是
价,最高化合价是 价,那么根据下列物质中Br元素的化合价判断,下列物质中只具有氧化性的是
价,那么根据下列物质中Br元素的化合价判断,下列物质中只具有氧化性的是
A.NaBr B.KBrO3 C.NaBrO D.HBrO4
第II卷(非选择题 共52分)
注意:1、答第II卷5-8页用钢笔或圆珠笔将答案直接写在试题卷上。
15.将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+物质的量之比是
A.3:2 B.2:3 C.1:2 D.1:1
14.氢氧化钡溶液中滴入等物质的量浓度的硫酸溶液并测定溶液导电性,下面各图表示的是随着硫酸滴入量的增加溶液导电能力变化的图像,其图像表示正确的是(横坐标为硫酸滴入量,纵坐标为导电性)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com