

题目列表(包括答案和解析)
14、下列关于氧化还原反应的叙述中正确的是 ( )
A.氧化还原反应的本质是化合价的升降,特征是电子的得失或电子对的偏移
B.一部分复分解反应可能是氧化还原反应
|
C.在反应2H2O = H2↑ + O2↑中,水既是氧化剂又是还原剂
D.在氧化还原反应中氧化剂得到电子发生氧化反应,还原剂失去电子发生还原反应
13、下列各组离子,能在溶液中大量共存的是 ( )
A. B. Ba2+、
B. Ba2+、 、
、 、
、
C.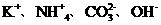 D .H
D .H 、
、 、NO3-、HCO3-
、NO3-、HCO3-
12、下列关于蒸馏操作要点及原因中,正确的是 ( )
A.蒸馏烧瓶可以直接加热,不用垫石棉网
B.温度计水银球插入蒸馏的混合液中,以控制蒸馏的温度
C.冷凝管中冷却水与被冷凝蒸气或液体流向相反,增强冷凝效果
D.烧瓶内放些碎瓷片以免爆炸。
11、下列离子方程式中正确的是 ( )
A.锌片插入硝酸银溶液中:Zn+Ag+ = Zn2++Ag
B.往碳酸钙中滴加稀盐酸:CO32 -+2H+=CO2↑+H2O
C.稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑
D.氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl-
10、 有关实验的叙述,正确的是 ( )
A.将固体加入容量瓶中溶解并稀释至刻度,即可配制成一定物质的量浓度的溶液
B.从100ml硫酸溶液中取出10mL,则这10mL溶液的物质的量浓度为原来的十分之一
C.98g硫酸溶于1L水,所得溶液的物质的量浓度为1mol/L
D.将8.0g硫酸铜配成500mL溶液,所得硫酸铜溶液的浓度为0.1mol/L
9、现有一瓶甲和乙的混合物,已知甲和乙的某些性质如下:
|
物质 |
熔点 |
沸点 |
密度 |
水中的溶解性 |
|
甲 |
-98℃ |
47.7℃ |
0.93g/mL |
可溶 |
|
乙 |
-84℃ |
77℃ |
0.90g/mL |
可溶 |
据此,将甲和乙相互分离的最佳方法是 ( )
A.萃取法 B. 过滤法 C.蒸馏法 D.分液法
7、关于氢氧化铁胶体和氯化镁溶液的说法中正确的是 ( )
A.可用丁达尔现象区分氢氧化铁胶体和氯化镁溶液两种分散系
B.两者的分散质微粒均能透过半透膜和滤纸
C.将氢氧化铁固体和氯化镁固体分别溶于水中即可得到氢氧化铁胶体和氯化镁溶液
D.两种分散系中的分散质微粒直径均介于1-100nm之间
8、能用离子方程式H++OH-=H2O表示的反应是 ( )
A.盐酸和氨水反应 B.稀硫酸和烧碱溶液反应
C.稀盐酸和氢氧化铜反应 D.稀硫酸和氢氧化钡溶液反应
6、设NA代表阿伏加德罗常数的数值,下列说法正确的是 ( )
A.22.4 L 中含有NA个
中含有NA个 分子
分子
B.标准状况下,22.4L水中的分子数为NA
C.1 L 0.1 mol·L-1 溶液中有0.1NA个Na+
溶液中有0.1NA个Na+
D.NA个一氧化碳分子和0.5 mol水的质量比为28 :9
5、下列说法不正确的是 ( )
A.除去粗盐中的泥沙的提纯步骤为:溶解、过滤、蒸发,且三步中都要用到玻璃棒
B.过滤时,玻璃棒与三层滤纸的一边接触,漏斗下端紧贴烧杯内壁
C.加热蒸发氯化钠溶液时,一直加热到水全部蒸干为止
D.过滤时玻璃棒的作用是引流,蒸发时玻璃棒的作用是搅拌使之受热均匀
4、关于物质的分类正确组合是 ( )
|
分类 组合 |
酸 |
碱 |
盐 |
氧化物 |
|
A |
H2SO4 |
Na2CO3 |
NaHCO3 |
SiO2 |
|
B |
HCl |
NaOH |
NaCl |
Na2O |
|
C |
CO2 |
NaOH |
MgCl2 |
SO3 |
|
D |
HNO3 |
KOH |
CaO |
CaCO3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com