
题目列表(包括答案和解析)
19. 如图3所示,用三块完全相同的两面平行的玻璃板组成一等边三角形(中间是空气),有红光和蓝光组成一细光束以平行底边BC从AB面射入,由AC面射出,则从AC面射出的光束( )
如图3所示,用三块完全相同的两面平行的玻璃板组成一等边三角形(中间是空气),有红光和蓝光组成一细光束以平行底边BC从AB面射入,由AC面射出,则从AC面射出的光束( )
A.分成两束,上面为红光,下面为蓝光
B.分成两束,上面为蓝光,下面为红光
C.仍然为一束,并与底边BC平行
D.仍然为一束,但向底边BC偏折
18.一定质量的气体(分子力及分子势能不计)处于平衡状态Ⅰ,现设法使其温度降低同时压强增大,达到平衡状态Ⅱ,则在状态Ⅰ变为状态Ⅱ的过程中 ( )
A.气体分子的平均动能必定减小
B.单位时间内气体分子对器壁单位面积的碰撞次数增多
C.气体的内能可能不变
D.气体必定放出热量
17.有两个行星A和B(A和B之间的相互作用不计),它们各有一颗靠近其表面的卫星,若这两颗卫星的周期相等,由此可知( )
A.行星A、B表面重力加速度之比等于它们的半径之比
B.两颗卫星的线速度一定相等
C.行星A、B的质量一定相等
D.行星A、B的密度不一定相等
16.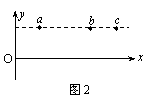 如图2所示,a、b、c表示某时刻一简谐横波的波动图象与一条平行于x轴的直线相交的三个质点,关于这三个质点的运动情况,下列说法正确的是 ( )
如图2所示,a、b、c表示某时刻一简谐横波的波动图象与一条平行于x轴的直线相交的三个质点,关于这三个质点的运动情况,下列说法正确的是 ( )
A.该时刻这三个质点一定具有相同的加速度
B.该时刻这三个质点一定具有相同的速度
C.任意时刻这三个质点相对于平衡位置的位移都相同
D.经过任意时间,这三个质点通过的路程都相同
15.如图1所示,理想变压器原线圈输入交变电压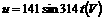 ,副线圈接有一电流表和阻值为100Ω的负载电阻R,测得电流表的示数为0.10A。由此可知该变压器的原、副线圈的匝数比为(
)
,副线圈接有一电流表和阻值为100Ω的负载电阻R,测得电流表的示数为0.10A。由此可知该变压器的原、副线圈的匝数比为(
)
A.141∶1 B.14.1∶1 C.100∶1 D.10∶1
14.一群处于基态的氢原子吸收了能量Eo的光子后,释放出多种能量的光子,其中有一种光子的能量为E1,则下列说法正确的是 ( )
A.E1一定不大于Eo B.E1一定不小于Eo
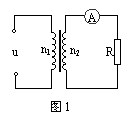 C.E1一定小于Eo D.E1一定等于Eo
C.E1一定小于Eo D.E1一定等于Eo
12.在一容积恒定密闭容器中,等物质的量的A和B发生如下反应:A(g)+2B(g)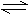 2C(g),一段时间后反应达到平衡,若同温度下所得混合气体压强是原来的4/5,则这时A的转化率是
( )
2C(g),一段时间后反应达到平衡,若同温度下所得混合气体压强是原来的4/5,则这时A的转化率是
( )
A.40% B.50% C.60% D.70%
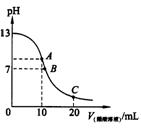 13.25℃时,在20ml
0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )
13.25℃时,在20ml
0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )
A.在A点: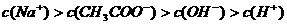
B.在B点: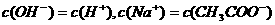
C.在C点: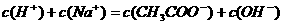
D.在C点: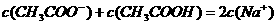
11.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l) Zn(OH)2
(s)+Mn2O3(s)下列说法错误的是 ( )
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-=Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
10.1g 氢气在氧气中完全燃烧生成气态水时,放出热量120.9kJ。则下列说法正确的是 ( )
A.反应的热化学方程式:2H2(g)+O2(g)=2H2O(g);△H=+483.6kJ·mol-1
B.氢气的燃烧热为241.8 kJ·mol-1
C.1molH2O(1)的能量大于1molH2O(g)的能量
D.2molH2和1molO2的能量总和大于2molH2O(g)的能量
9.14C是碳的一种同位素原子。设N0为阿伏加德罗常数值,下列说法
不正确的是 ( )
A.1/8 mol 14CH4分子所含中子数为N0
B.7 g 14C原子形成的石墨完全燃烧生成二氧化碳时所转移的电子数为2N0
C.常温常压下,22.4 L含14C的二氧化碳中分子数等于N0
D.常温常压下,17 g甲基(-14CH3)所含电子数为9N0
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com