
题目列表(包括答案和解析)
6、能正确表示下列化学反应的离子方程式的是
A、硫酸和氢氧化钡溶液反应 H++OH-=H2O
B、澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C、铜片插入硝酸银溶液中 Cu + 2Ag+ = Cu2+ +2 Ag
D、碳酸钙溶于稀盐酸中 CO32-+2H+=H2O+CO2
5、在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A、Na+、K+、SO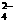 、Cl- B、Na+、Cu2+ 、SO
、Cl- B、Na+、Cu2+ 、SO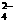 、NO
、NO
C、Fe3+、Na+、SO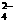 、NO3- D、Ba2+、HCO
、NO3- D、Ba2+、HCO 、NO
、NO 、K+
、K+
4、设NA为阿伏加德罗常数,下列说法中正确的是
A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
B、54g H2O中含有3NA个水分子
C、标准状况下, NA个水分子所占的体积为22.4L
D、1mol 氢中所含的原子数为NA
3、“假说”在化学科学的研究和发展中起到不可替代的作用。下列“假说”在化学科学发展过程中曾经起到一定的作用,从目前的化学理论看,仍然科学的是 A、道尔顿提出的“每一元素的原子以其原子质量为其特征” B、阿伦尼乌斯提出的“电解质在溶液中会自发离解成带电的粒子” C、贝采里乌斯提出的“不同原子带不同的电性,因而产生吸引力,由此形成化合物” D、盖·吕萨克提出的“在同温同压下,相同体积的不同气体含有相同数目的原子”
2、aXn-和bYm+两种简单离子,其电子层结构相同,下列关系式或化学式正确
A、a – n = b + m B、a + m = b – n
C、氧化物为YOm D、氢化物为HXn或XnH
1、下列仪器常用于物质分离的是



 ① ② ③ ④
① ② ③ ④
A、②③ B、①④ C、②④ D、①②
16.(12分)现欲配制100 mL 1.0 mol/L的硫酸铜(CuSO4)溶液,试求:
(1) 若用无水硫酸铜配制,则需要无水硫酸铜粉末的质量是多少?
(2) 若用5.0 mol/L CuSO4溶液配制,则需要该溶液多少毫升?
(3) 若用胆矾(CuSO4 5H2O)配制,则需要胆矾的质量是多少?
15.(20分)为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
 (1)判断BaCl2已过量的方法是
。
(1)判断BaCl2已过量的方法是
。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
; ___________________________________.
 (3)在 中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
(3)在 中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
(4)从实验设计方案优化的角度分析步骤②和④可否颠倒____________(填“是”或“否”,如果“否”,请说明理由。)原因是:_______________________________________________;
步骤③和④可否颠倒____________。
(5)若先用盐酸再进行操作⑤,将对实验结果产生影响,其原因是:
__________ 。
14.(16分)右图为实验室某浓盐酸试剂瓶标签上的有关数据,
|
⑴该浓盐酸中HCl的物质的量浓度为___________ mol·L-1 。
⑵取用任意体积的该盐酸溶液时,下列物理量中不随所取体
积的多少而变化的是_______________。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
⑶某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.400 mol·L-1的稀盐酸。
①该学生需要量取____________ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(在空格中填 “偏大”、填 “偏小”或“无影响”)。
I、定容时俯视观察凹液面______________;
II、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_______________。
13. (16分)掌握仪器的名称、组装及使用方法
(16分)掌握仪器的名称、组装及使用方法
是[C2] 中学化学实验的基础,下图为两套实验装置。
⑴写出下列仪器的名称:
①____________;②_____________;
④__________; I II
⑵仪器①-④中,使用时必须检查是否漏水的有______。(填序号)
⑶若利用装置I分离四氯化碳和乙醇的混合物,还缺少的仪器是_________,将仪器补充完整后进行的实验操作的名称为_____________ 。现需配制250 mL 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是______________、_________________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com