
题目列表(包括答案和解析)
22.(18分)(1)(6分)螺旋测微器的旋钮旋转一周,螺杆前进或后退_________mm,可动刻度共分_________
 等份。现用它测量金属丝的直径,如图甲所示,则此金属丝的直径是_________mm
等份。现用它测量金属丝的直径,如图甲所示,则此金属丝的直径是_________mm
(2)(12分)要精确测量一个阻值约为5Ω 的电阻丝的电阻Rx,实验提供下列器材:电流表A1:量程100mA,内阻r1约为4Ω; 电流表 A2:量程500μA,内阻r2 = 750Ω;直流电源E:电动势E=2V,内阻很小;变阻器R0:阻值10Ω;开关S,导线若干。
①请在方框中画出测定电阻Rx的电路图,并表明器材代号。(4分)
②根据你设计的电路图,将图乙中的实物连成实验电路。(4分)
③根据某次测量的结果写出电阻Rx的表达式,Rx =__________式中各符号的意义是______________________________________________(4分)
23.(16分)在用高级沥青铺设的高速公路上,汽车的设计时速是108km/h。汽车在这种路面上行驶时,它的轮胎与地面的最大静摩擦力等于车重的0.6倍。如果汽车在这种高速路的水平弯道上拐弯,假设弯道的路面是水平的,其弯道的最小半径是多少?如果高速路上设计了圆弧拱桥做立交桥,要使汽车能够安全通过圆弧拱桥,这个圆弧拱桥的半径至少是多少?(取g=10m/s2)
24. (18分) 光滑导轨宽L=50cm,导轨间有垂直于导轨平面、方向向里的匀强磁场,磁感应强度B=1T,垂
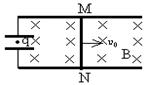 直导轨放有一导体棒MN.导轨左端接有极板水平的平行板电容器,其两极间
直导轨放有一导体棒MN.导轨左端接有极板水平的平行板电容器,其两极间
的距离为d=20cm,如图所示.当导体棒以速度υ0=2m/s沿导轨向右匀速运动
时,电容器极板正中间一质量m=10-8kg的带电微粒正好静止.(不计空气阻
力,取g=10m/s2)求:⑴带电微粒的电性和电荷量.⑵如果将电容器的下极
板瞬间降低20cm(不考虑瞬间过程中的变化),则带电微粒将向哪一块极板动?到达极板时的速度是多少?
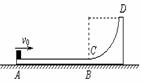
25.(20分)如图所示,竖直平面内的轨道ABCD由水平轨道AB与光滑的四分之一圆弧轨道CD组成,AB恰与圆弧CD在C点相切,轨道固定在水平面上。一个质量为m的小物块(可视为质点)从轨道的A端以初动能E冲上水平轨道AB,沿着轨道运动,由DC弧滑下后停在水平轨道AB的中点。已知水平轨道AB长为L。求:
 (1)小物块与水平轨道的动摩擦因数
(1)小物块与水平轨道的动摩擦因数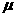 。
。
(2)为了保证小物块不从轨道的D端离开轨道,圆弧轨道的半径R至少是多大?
(3)若圆弧轨道的半径R取第(2)问计算出的最小值,增大小物块 的初动能,使得小物块冲上轨道后可以达到最大高度是1.5R处,试求物块的初动能并分析物块能否停在水平轨道上。如果能,将停在何处?如果不能,将以多大速度离开水平轨道?
26.(14分)某透明溶液中可能有NH4+、Na+、Mg2+、Fe2+、Al3+、Cu2+、CO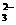 、NO3-、Cl-中的一种或几种。取该种溶液少许,加入NaOH溶液并加热,观察到白色沉淀生成并伴有刺激性气味的气体产生。沉淀过滤后,在沉淀中继续加入过量NaOH溶液,白色沉淀部分溶解,试回答下列问题:
、NO3-、Cl-中的一种或几种。取该种溶液少许,加入NaOH溶液并加热,观察到白色沉淀生成并伴有刺激性气味的气体产生。沉淀过滤后,在沉淀中继续加入过量NaOH溶液,白色沉淀部分溶解,试回答下列问题:
(1)实难中产生的气体是: (填分子式);
(2)原溶液中一定含有离子是: ;可能含有的阳离子是: ;验证该离子存在的方法是 ;
(3)原溶液中一定不含有的离子是: ;
(4)在沉淀中继续加入NaOH溶液,沉淀部分溶解,发生反应的离子方程式为: ;
27.(15分)在一定条件下,下列物质间可发生如下图所示的转化:
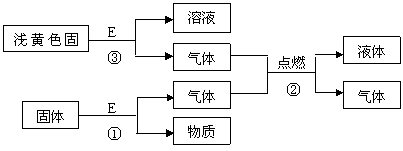
请填写下列空白:
(1)写出W的电子式 。
(2)若乙是制氯乙烯的基础原料,反应①的化学方程式为:____________ 。已知乙的燃烧热为1294.8KJ/mol,表示乙燃烧热的热化学方程式为 。试写出过量的丙通入C(悬浊液状态)中的离子反应方程式:_____ 。
(3)若乙是碱性气体,A由短周期元素组成,则A的化学式为___________ 。
28.(15分)已知: 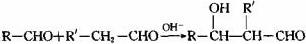 ,有机物G属于酯类,其分式为C20H18O4,合成G的路线如下图,其中C的分子式为C9H8O2
,有机物G属于酯类,其分式为C20H18O4,合成G的路线如下图,其中C的分子式为C9H8O2
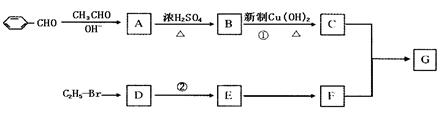
请回答下列问题。
(1)写出下列物质的结构简式:A F 。
(2)反应类型:① ②
(3)写出下列化学反应方程式。
①C2H5-Br-→D: ②B-→C:
(4)写出有机物C的所有与C具有相同官能团的同分异构体(不包括C)
、 、 、 。
29.(16分)某校化学课外活动小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2%NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3块状固体 ⑦K2CO3粉末
仪器装置(如下图所示)
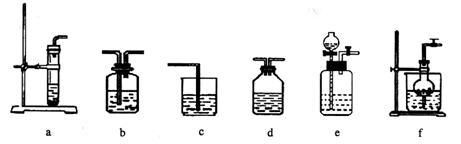
若用X代表制备过程中可随开随用的气体发生装置图,Y代表除杂洗气装置,Z代表制备产品的装置。试按要求回答下列问题:
(1)制取CO2气体的发生装置图可选用 ;但要使制备过程做到随开随用,只能选用 ;(填字母编号)
(2)除杂装置可先用 (填字母编号),装置内的试剂应选用 (填字序号),除去的杂质为 (填化学式)
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为__________________________________,Y装置中除去杂质为__________________________________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是_____________。若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过____%(质量分数)。(小数点后保留1位有效数字)
附:有关物质的常温(20℃)时的溶解度
|
化学式 |
Na2CO3 |
NaHCO3 |
NaOH |
NaCl |
Na2SO4 |
|
溶解度(g/100g) |
21.3 |
9.6 |
107 |
35.8 |
19.4 |
30.(一)(8分)人的唾液淀粉酶作用于某种物质(底物)。温度和PH保持最适值,生成物量与反应时间关系如下图。
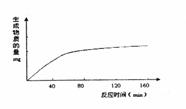 (1)该酶作用后的产物是 。如将溶液的PH
(1)该酶作用后的产物是 。如将溶液的PH
由2逐渐调到10,生成物的量将 。
(2)若增加酶浓度,其他条件和底物浓度不变,请
在原图上划出生成物质量的变化曲线。
(3)下列哪些物质与该酶的本质相同 。
①抗毒素 ②淋巴因子 ③神经递质的受体
④生长素 ⑤噬菌体的衣壳
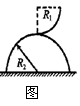
21.如图2,从光滑的1/4圆弧槽的最高点滑下的小物块,滑出槽口时速度为水平方
向,槽口与一个半球顶点相切,半球底面为水平,若要使小物块滑出槽口后不沿半
球面下滑,已知圆弧轨道的半径为R1,半球的半径为R2,则R1与R2的关系为( )
A.R1≤R2 B.R1≥R2 C.R1≤R2/2 D.R1≥R2/2
20.如图所示,两条水平虚线之间有垂直于纸面向里,宽度为d,磁感应强度为B的匀强磁场.质量为m,电
阻为R的正方形线圈边长为L(L< d),线圈下边缘到磁场上边界的距离为h.将线圈由静止释放,其下边
 缘刚进入磁场和刚穿出磁场时刻的速度都是v0,则在整个线圈穿过磁场的全过程中 (从下边缘进入磁场到
缘刚进入磁场和刚穿出磁场时刻的速度都是v0,则在整个线圈穿过磁场的全过程中 (从下边缘进入磁场到
上边缘穿出磁场),下列说法中正确的是
A.线圈可能一直做匀速运动
B.线圈可能先加速后减速
C.线圈的最小速度一定是mgR/B2L2
 D.线圈的最小速度一定是
D.线圈的最小速度一定是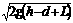
19.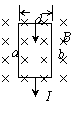 金属导体板宽为d,通以如图所示方向的电流,其中自由电子定 向运动的速度为v,整个导体板置于磁感
金属导体板宽为d,通以如图所示方向的电流,其中自由电子定 向运动的速度为v,整个导体板置于磁感
应强度为B的匀强磁场中。则下面说法正确的是 ( )
A.导体左侧聚集较多的电子,使右侧的电势高于左侧的电势
B.导体右侧聚集较多的电子,使左侧的电势高于右侧的电势
C.由于电子的聚集,使得左右两侧电势差为2Bdv
D.由于电子的聚集,使得左右两侧电势差为Bdv
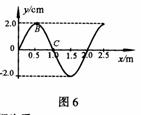
18.如图是一个由电池、电阻和可调电容器组成的串联电路,转动可调电容
器的动片使极板间正对面积减小的过程中,下列说法正确的是
A.电容器的电容变大 B.电容器的电容变小
C.电阻中有从M流向N的电流 D.电阻中有从N流向M的电流
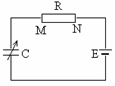
17.图6是一列向x轴正方向传播的简谐横波在t = 0时刻的波形图,此时质点B
恰好运动到波峰,质点C恰好通过平衡位置。若该波的周期为4.0s,则
对质点B和C下列说法中正确的是
A.它们开始振动时的运动方向不相同
B.它们在开始振动的第一秒内加速度方向均一定沿y 轴正方向
C.在开始振动后的任何连续的2s内,回复力对它们做的功都为零
 D.它们振动过程中的任意1s内通过路程均为2.0cm
D.它们振动过程中的任意1s内通过路程均为2.0cm
16. 如图5所示,放在粗糙水平桌面上的木块,质量m = 2.0kg,同时受到F1 =8.0N、F2 =3.0N的水平推力作用处于静止状态。若只撤去F1,则木块
如图5所示,放在粗糙水平桌面上的木块,质量m = 2.0kg,同时受到F1 =8.0N、F2 =3.0N的水平推力作用处于静止状态。若只撤去F1,则木块
A.向左做匀速运动 B.仍处在静止状态
C.以a = 1.0m/s2的加速度向右做匀加速运动
 D.以a = 1.5m/s2的加速度向左做匀加速运动
D.以a = 1.5m/s2的加速度向左做匀加速运动
15.下列说法中正确的是
A.布朗运动是液体分子对悬浮颗粒的碰撞作用不平衡造成的
B.容器中的气体对器壁的压强是由于大量气体分子频繁撞击器壁而产生的
C.若两个分子只受到它们间的分子力作用,在两分子间距离增大的过程中,分子的动能一定增大
D.用N表示阿伏德罗常数,M表示铜的摩尔质量,ρ表示铜的密度,那么一个铜原子所占空间的体积可表示为M/(ρN)
14.许多物理现象在科学技术领域得到应用,以下说法中正确的是
A.医院里常用X射线对病房和手术室进行消毒
B.照相机镜头表面涂上增透膜,以增强透射光的强度,是应用了光的全反射现象
C.利用红外线进行遥感、遥控,主要是因为红外线的波长大,不容易发生衍射
D.明线光谱和暗线光谱都可以用来分析物质的组成成分
13.对于白磷引起的中毒,硫酸铜溶液是一处解毒剂,有关反应如下:
11P + 15CuSO4 + 24H2O ====5Cu3P +6H3PO4 + 15H2SO4 下列关于该反应的说法正确的是
A.CuSO4发生了氧化反应 B.生成1 mol H3PO4时,有10 mol 电子转移
C.氧化产物和还原产物的物质的量之比6:5 D.白磷只作还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com