
题目列表(包括答案和解析)
8、D 解析:A不正确,如SO2通入水中溶液能导电,但电解质是H2SO3。B不正确。如HCl是电解质,但液态HCl不导电,因为HCl在熔融状态下不能生成可以自由移动的离子。C错误。D是电解质的定义,故正确。
7、B 解析:A中的MnO 在水溶液中显紫色;C中的Cu2+在水溶液中显蓝色;D中要发生离子反应Ba2+’+SO
在水溶液中显紫色;C中的Cu2+在水溶液中显蓝色;D中要发生离子反应Ba2+’+SO
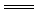 BaSO4↓,故答案应选B,只有B符合要求。
BaSO4↓,故答案应选B,只有B符合要求。
6、D 解析:A中可发生离子反应H++OH-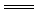 H2O及Mg2++2OH-
H2O及Mg2++2OH-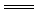 Mg(OH)2↓;B中可以发生反应Ba2++CO
Mg(OH)2↓;B中可以发生反应Ba2++CO
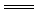 BaCO3↓;C中可发生反应CO
BaCO3↓;C中可发生反应CO +2H+
+2H+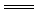 H2O+CO2↑;D各离子相互之间不能发生反应,故应选D。
H2O+CO2↑;D各离子相互之间不能发生反应,故应选D。
5、D解析:A中的CaCO3不能拆成离子形式;B中反应的离子方程式为:Ba2++2OH-+2H++SO
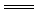 BaSO4↓+2H2O;C的离子方程式不符合客观事实;D是正确的。
BaSO4↓+2H2O;C的离子方程式不符合客观事实;D是正确的。
4、CD解析:各选项所对应的离子方程式为:A.Ba2++2OH-+2H++SO
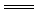 BaSO4↓+2H2O B.Fe(OH)3+3H+
BaSO4↓+2H2O B.Fe(OH)3+3H+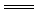 Fe3++3H2O C、D:H++OH-
Fe3++3H2O C、D:H++OH-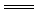 H2O
H2O
3、 BC 解析:电解质是指在水溶液中或熔融状态下能够导电的化合物。题目中只有B和C是符合条件的,其中HCl在水溶液中可以导电,BaSO4在熔融状态下可以导电。NaOH溶液是混合物;CO2通入水中虽可以导电,但原因是生成了H2CO3,H2CO3是电解质。故答案应选B、C。
BC 解析:电解质是指在水溶液中或熔融状态下能够导电的化合物。题目中只有B和C是符合条件的,其中HCl在水溶液中可以导电,BaSO4在熔融状态下可以导电。NaOH溶液是混合物;CO2通入水中虽可以导电,但原因是生成了H2CO3,H2CO3是电解质。故答案应选B、C。
2、AD 解析:电解质溶液的导电能力取决于溶液中的离子浓度。离子浓度大则导电能力强。题中B、C反应后离子浓度变化不大,所以导电性变化不大,A、D中加入NaOH没有化学反应发生,但离子浓度变化较大。
1、D 解析:固态氯化钾不导电,因为无自由移动的离子。
16.某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH-、NO 六种离子。
六种离子。
 (1)甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是________、________、________。
(1)甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是________、________、________。
(2)乙厂的废水中含有另外三种离子。如果加一定量________(选填“活性炭”“铁粉”),可以回收其中的________(填写金属元素符号)。
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的________(填写离子符号)转化为沉淀。经过滤后的废水主要含________,可用来浇灌农田。
答案及详解:
15.(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:__________。
(2)在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:__________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com