
题目列表(包括答案和解析)
14.向一定量FeO、Fe和Fe3O4的混合物中加入100mL1.0 mo1·L-1的盐酸,使混合物完全溶解,放出224mL(标准状况)气体,再向反应后的溶液中加入1 mo1·L-1NaOH溶液,要使铁元素完全沉淀下来,所加入NaOH溶液的体积最少为( )
A.90mL B.100mL C.150mL D.200mL
13.合金相对纯金属制成的金属材料来说优点是( )
①合金的硬度一般比它的各成分金属的大
②一般合金的熔点比它各成分金属的更低
③改变原料的配比,改变生成合金的条件,可得到具有不同性能的合金
④合金比纯金属的导电性更强
⑤合金比纯金属的应用范围更广泛
A.①②③⑤ B.②③④ C.①②④ D.①②④⑤
12.粗盐中往往含有可溶性的CaCl2、MgCl2及一些硫酸盐,常常加入一些化学试剂,使一些可溶性的杂质沉淀下来,过滤后除去同时采用必要的操作步骤,下列操作顺序正确的是( )
①加BaCl2 ②加NaOH ③加Na2CO3 ④加稀HCl ⑤过滤
A.①②③④⑤ B.⑤④③②① C.①②③⑤④ D.③①②⑤④
11.某溶液中有①NH4+②Mg2+③Fe2+④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是( )
A.只有② B.只有④ C.①③ D.①②③④
10.下列检验方法不正确的是( )
A.向溶液中加入盐酸酸化的BaCl2溶液检验SO42-的存在
B.先取少量溶液,加入盐酸放出无色无味使澄清石灰水变浑浊的气体,再取少量溶液加入BaCl2溶液,若产生白色沉淀则说明有CO32-存在
C.向溶液中滴加KSCN产生血红色溶液说明有Fe3+存在
D.物质进行焰色反应时,透过蓝色的钴玻璃观察有紫色火焰说明有钾元素存在
9. 磁流体是电子材料的新秀,它既有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可产生黑色的、分散质粒子的直径为5.5nm~36nm的磁流体,下列说法中正确的是( )
磁流体是电子材料的新秀,它既有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可产生黑色的、分散质粒子的直径为5.5nm~36nm的磁流体,下列说法中正确的是( )
A.所得到的分散系为浊液
B.用一束光照射该分散系,可以看到一条光亮的“通路”
C.该分散系的分散质为Fe(OH) 3
D.该分散系极不稳定
8.菜谱中记载:河虾不宜与西红杮同食,主要原因是河虾中含有+5价砷,西红杮中含有比较多的维生素C,两者同食会产生有毒的+3价砷,下列说法中正确的是( )
A.在该反应中维生素C作催化剂
B.在该反应中维生素C作氧化剂
C.因为河虾中含有砷元素,所以不能食用
D.河虾与西红杮同食时发生了氧化还原反应
7.实验室配制一定物质的量浓度的溶液时,需用到容量瓶,容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以向容量瓶中转移液体时,需一定的耐心和技巧,有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是( )
A.可以按此建议改进,因为可在使用容量瓶时带来方便
B.不能按此建议改进,因为会降低容量瓶的精度
C.如果加粗瓶颈,可将原刻在容量瓶瓶颈上的刻度改刻在容量瓶的瓶身上
D.不必加粗瓶颈,因为向容量瓶中转移液体时,少量液体倒出瓶外,不会对溶液的浓度产生影响
6.在化学研究中,溶液组分的表示还有两种方法:
①质量物质的量浓度=
②物质的量分数= ×100%
×100%
在某温度范围内,溶液状态不发生变化,下列对某溶液组分的表示方法中受温度影响的是( )
A.质量分数 B.物质的量浓度
C.质量物质的量浓度 D.物质的量分数
5.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是( )
 A.
A. 、
、 、
、 、
、 B.
B. 、
、 、
、 、
、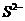
C. 、
、 、
、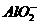 、
、 D.
D. 、
、 、
、 、
、
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com