
题目列表(包括答案和解析)
22、(10分)某同学要配制1.0 mol/L的NaOH溶液,提供的仪器有
①容量瓶(250mL) ②玻璃棒 ③托盘天平(配砝码和镊子) ④药匙 ⑤胶头滴管 ⑥烧杯 ⑦漏斗
(1)上述仪器中配制溶液时所需的玻璃仪器有 (填序号),容量瓶上标有①温度 ②浓度 ③容量 ④压强 ⑤刻度线 五项中的 (填序号)。
(2)用托盘天平和小烧杯称取NaOH时,有下列操作步骤,正确的顺序是
(有的操作可重复使用)
A﹒调整天平零点 B﹒将砝码放回砝码盒中,将游码拨回零刻度
C﹒称取小烧杯的质量 D﹒称取小烧杯和NaOH的质量
E﹒记录称量的数据
(3)由题意可知,你应该称取固体NaOH g,如果由于称量时间过长,你所
配制的NaOH溶液的浓度与要求相比 (填“偏大”“偏小”“相等”) 。
21、 (6分)已知:甲、乙、丙为常见单质,甲常温下为固体,乙为一黄绿色气体,丙为无色气体。A、B、C、D均为化合物,A的水溶液遇KSCN溶液变红色,它们之间有下图转化关系。请回答以下问题。
(6分)已知:甲、乙、丙为常见单质,甲常温下为固体,乙为一黄绿色气体,丙为无色气体。A、B、C、D均为化合物,A的水溶液遇KSCN溶液变红色,它们之间有下图转化关系。请回答以下问题。
(1)写出下列物质的化学式:乙 ;B 。
(2)写出③反应的化学方程式: 。
(3)写出②反应的离子方程式: 。
20、(6分)在某NaOH溶液里加入几滴酚酞试液,溶液显红色,向其中缓缓通入SO2气体,溶液红色渐渐褪去。回答下列问题:
(1)产生该现象的原因可能有:
① ;
② 。
(2)简述怎样用实验证明红色褪去的原因是①或者是②。
。
19、(11分)为检验一纯净物是否为 (NH4)2SO4 ,取少量该固体溶于水,把溶液分成三份置于试管中。请完成下列实验过程,要求写出每步实验的现象和结论。
(1)在一份溶液中加入
;反应的离子方程式为 。
(2)在第二份溶液中加入
;反应的离子方程式为 。
(3)在第三份溶液中加入 ,若无
现象,则表明原固体中不含 离子。
结合(1)(2)(3),可确定该纯净物为 (NH4)2SO4 。
18、(6分) 氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 ======
======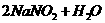
在该反应中,氧化剂是 。
(2)汽车尾气中含有一氧化氮和一氧化碳,经过排气管中的催化转化器转化为对人体无毒害作用的物质。写出该反应的化学方程式: 。
(3)在一定条件下氨气亦可用来将氮氧化物转化为无污染的物质。写出氨气和二氧化氮在一定条件下反应的化学方程式: 。
17、(4分)在铝制易拉罐中收集一满罐CO2,加入过量浓氢氧化钠溶液,立即把口封闭。可以发现易拉罐“咔咔”作响,并变瘪了,写出发生反应的离子方程式 ;过一会儿后,易拉罐又会作响并鼓起来,写出发生反应的离子方程式 。
16、将足量的铜屑加入到浓度均为1 mol/L 的HNO3 和H2SO4 的混合溶液100 mL中,充分反应后,转移电子的物质的量为:
A、0.45 mol B、0.225 mol C、0.15mol D、0.075mol
15、铜粉加入稀盐酸中,加热无现象,这时加入一种盐则铜粉溶解而溶液变蓝,同时有气体放
出,这种盐是:
A、Fe2(SO4)3 B、NaCl C、FeCl2 D、KNO3
14、一定质量的铝铁合金溶于足量的盐酸中,完全反应后产生5.6 L(标准状况下)气体;用同样质量的铝铁合金溶于足量的NaOH溶液中,在标准状况下产生3.36 L气体,则该合金中铝、铁的物质的量之比为:
A、1∶1 B、2∶5 C、3∶2 D、3∶5
13、在氯水中存在多种分子和离子,可通过实验的方法加以确定。下列说法不正确的是:
A、氯水呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在
B、放入有色布条后,有色布条褪色,说明有HClO分子存在
C、加入含有NaOH的酚酞试液,红色褪去,说明有H+离子存在
D、加入硝酸酸化的AgNO3溶液,产生白色沉淀,说明有Cl-离子存在
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com