
题目列表(包括答案和解析)
1.下列变化中不属于化学变化的是 ( )
A.SO2使品红溶液褪色 B.活性碳使红墨水褪色
C.氯水使有色布条褪色 D.漂白粉使某些染料褪色
23.(10分)钠和过氧化钠的混合物加入到足量的水中生成的混合气体点火爆炸,恰好完全反应,则:
(1)原混合物中Na、Na2O2的物质的量比是多少?
(2)原混合物中Na、Na2O2的质量比是多少?
22.(16分)A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)

|
|
|
|
 A B C
A B C
试回答下列问题:
(1)若X是强氧化性气体单质,则A可能是 ________________(填序号)
a.C b.Al c.Na d.Mg
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在A中燃烧产生棕黄色的烟
①B的化学式为________________,C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)________________________________________。
②向C的溶液中加入氢氧化钠溶液,现象是_______________________________,涉及的氧化还原反应的化学方程式为__________________________________。
(3)若A、B、C均为含有同种金属元素的化合物,X是强碱,则B的化学式为________,反应②的离子方程式为_______________________________。
21.(8分)在进行某实验探究过程中,一些学生发现等质量的铜片分别与等体积(均过量)的浓硝酸和稀硝酸反应,所得溶液前者为绿色,后者为蓝色。
(1)针对上述现象,学生们进行了讨论后,出现了以下两种观点:
一种认为,这可能是Cu2+浓度的差异引起的。你同意这种看法吗? (填“同意”或“不同意”),原因是 。
另一种认为,呈“绿色”是Cu2+与NO2混合的结果。请你设计出一个实验方案证明之,你设计的实验方案是
。
(2)请写出铜与稀硝酸反应的离子方程式,并标出电子转移的方向和数目:
。
20.(16分)下列是关于Cl2的制备和性质的系列实验,请回答有关问题。
|
MnO2+4HCl(浓)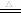 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
写出该反应的离子方程式_________________________________,指出该反应的还原剂:_________。产生11.2LCl2(标准状况),转移的电子物质的量是______。
(2)把红热的铜丝插入已收集满氯气的集气瓶中。
可观察的现象:_______________________________,
再往瓶中加入少量的水,振荡,溶液呈____色。该反应的化学方程式:______________,
(3)如果把干燥的氯气通入干燥的有色布条中,布条_____褪色,
(4)多余的氯气要用氢氧化钠溶液吸收,
写出该反应的离子方程式:_______________________________________,
(5)Cl2有____,该实验应在通风橱中进行。
19.(6分)已知下列反应:
①HPO3+H2O=H3PO4
②2Na2O2+2H2O=4NaOH+O2↑
③2F2+2H2O=4HF+O2
④2K+2H2O=2KOH+H2↑
⑤Cl2+H2O=HCl+HClO
(1)其中,H2O做氧化剂的是 ,H2O做还原剂的是 ,H2O既不是氧化剂又不是还原剂的是 。
(2)其中不属于氧化还原反应的是 。
18.质量比为2∶3的铝分别与足量的盐酸和足量的氢氧化钠溶液反应,放出氢气在相同条件下的体积比为
A.1∶1 B.1∶2 C.1∶3 D.2∶3
17.一定量的浓硝酸与过量的铜充分反应,生成的气体是
A.只有NO2 B.只有NO C.NO2和NO D.NO2和H2
16.用氯气消毒后的自来水配制下列溶液时,会使配制的溶液变质的是
①NaOH、②AgNO3、③Na2CO3、④FeCl2
A.②④ B.③④ C.②③④ D.全部
15.对于NaHCO3与Na2CO3的性质,下列叙述错误的是
A.质量相同时,跟足量的盐酸反应,在相同条件下Na2CO3产生的CO2气体多
B.物质的量相同时,跟足量的盐酸反应,Na2CO3所消耗H+的物质的量是NaHCO3的2倍
C.物质的量相同时,跟足量的盐酸反应,在相同条件下得到等体积的CO2
D.将它们分别加入到澄清石灰水中,都产生白色沉淀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com