
题目列表(包括答案和解析)
14.某溶液中含有大量的下列离子:Fe3+、SO42-、A13+和M离子,经测定Fe3+、SO42-、A13+和M离子的物质的量之比为2:4:1:1,则M离子可能是下列中的
A.Na+ B.OH- C.S2- D.C1-
13.下列反应的离子方程式书写正确的是
A.氯气和水的反应:C12+H2O=2H++C1-+ClO-
B.向A12(SO4)3溶液中加入过量的氨水:A13++3NH3·H2O=A1(OH)3↓+3NH4+
C.向硫酸溶液中加入Ba(OH)2溶液至中性:H++SO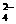 +Ba2++OH-=H2O+BaSO4↓
+Ba2++OH-=H2O+BaSO4↓
D.铜片加入稀硝酸中:3Cu+2NO3-+8H+=3Cu2++2NO2↑+4H2O
12.用NA 表示阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,22.4LCO2气体中含氧原子数目为2NA
B.1mo1·L-1的A1C13溶液中,C1-离子的数目为3 NA
C.任何条件下,23gNa+离子含有的最外层电子数为NA
D.60g的二氧化硅可与水反应生成硅酸的分子数为NA
11.在一定温度下,1 mol金属铜与足量某浓度的硝酸完全反应,生成NO2和NO的
物质的量之比为1:3,则反应过程中转移的电子总数为
A.2 mol B.3 mol C.4mol D.5 mo1
10.下列物质及对应的用途(括号内是用途)错误的是
A.硅(光导纤维) B.碘化银(人工降雨)
C.过氧化钠(呼吸面具中的供氧剂) D. 硫酸钡(钡餐)
9.下列实验方法不正确的是
A.用丁达尔现象鉴别颜色相似的浓溴水和Fe(OH)3胶体
B.用KMnO4溶液检验Fe2(SO4)3溶液中是否含有Fe2+
C.用等物质的量浓度盐酸可以鉴别Na2CO3和NaHCO3固体
D.用直接观察溶液灼烧的焰色可证明溶液中是否只含有Na+
8.酸雨是指
A.酸性的雨 B. pH<5.6的雨 C. pH=5.6的雨 D.pH<7的雨
7.氮化硅(Si3N4)是一种具有耐高温耐磨蚀等优异性能的新型陶瓷。工业上可用下列方法制取:3SiO2+6C+2N2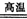 Si3N4+6CO。下列说法正确的是
Si3N4+6CO。下列说法正确的是
A.氮化硅陶瓷可用于制造汽车发动机
B.氮化硅是氧化产物
C.二氧化硅是还原剂[
D.氮化硅可改写成3SiO2·2NO2形式
6.下列电离方程式中,正确的是
A.H2SO4=H2++SO42- B.Ba(OH)2=Ba2++OH-
C.NaNO3=Na++NO3- D.HClO=H++Cl-+O2-
5.从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物;④将得到的产物熔融电解得到镁。下列说法不正确的是
A.此法的优点之一是原料来源丰富
B.①②③步骤的目的是从海水中获取MgCl2
C.提取镁的过程涉及化合、分解、置换反应
D.第④步电解时,还会产生副产品氯气
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com