
题目列表(包括答案和解析)
7.当光束通过下列分散系时,能观察到丁达尔效应的是
A.食盐溶液 B.盐酸 C. 胶体
D.硫酸铜溶液
胶体
D.硫酸铜溶液
6.用 表示阿伏加德罗常数,64g SO2含有的氧原子数为
表示阿伏加德罗常数,64g SO2含有的氧原子数为
A. B.
B.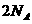 C.
C. D.
D.
5.Na2CO3俗称纯碱,下面的分类不正确的是
A.Na2CO3是碱 B.Na2CO3是盐
C.Na2CO3是钠盐 D.Na2CO3是碳酸盐
4.下列实验操作没有用到玻璃棒的是
A.溶解 B.萃取 C.过滤 D.蒸发结晶
3.当遇到氯气泄漏时,可行的方法是
A.躲到低洼的地方 B.顺风迅速撤离
C.多饮豆浆和牛奶 D.用肥皂水浸湿软布捂住口鼻
2.金属钠着火时,可用来灭火的是
A.CO2 B.沙土 C.煤油 D.水
1.下列气体中,不会造成空气污染的是
A.N2 B.Cl2 C.SO2 D.NO2
2.模块水平考试达60分,模块考试成绩为合格。
可能用到的相对原子质量:H 1 C 12 O 16 N 14 Mg 24 Al 27 S 32 Cl 35.5
Fe 56 Cu 64 Zn 65 Ba 137
模块水平测试
I卷(选择题,共50分)
(下列每个小题只有一个选项符合题意,请将符合题意的选项填写在机读卡。每小题2分,共25小题。)
2.将易拉罐剪开,用砂纸打磨使表面油漆和氧化膜去掉,再剪取一小块进行实验。
实验一:用胶头滴管向装有铝合金的大试管中加入足量的氢氧化钠溶液,可以看到有气泡生成,反应一段时间后,溶液中还有不溶物。
实验二:用滴管继续向实验一的试管中逐滴加入6mol/L的盐酸至足量,静置24小时。按实验顺序,该同学记录的现象如下:①开始没有明显现象;②有白色絮状沉淀生成;③白色沉淀消失;④原溶液中不溶物完全溶解,此时溶液呈浅绿色;⑤静置24小时后,溶液呈棕黄色
实验三:再向该试管中加入一定量的氢氧化钠溶液,最终只得到红棕色沉淀
请回答下列问题:
(1)本实验所配制的c(NaOH)_________c(HCl)(填“<”、“>”或“=”)。
(2)写出“实验一”中发生反应的化学方程式_______________________________________。
(3)实验二所得溶液为什么静置24小时后由浅绿色变为棕黄色?
________________________________________________________________________。
(4)写出“实验二”中产生①、②、③现象的反应离子方程式:__________________________、
__________________________________、_____________________________________。
(6)由此可知该假设_____________(填“成立”、“不成立” 或“无法确定”)。
1.配制20%(密度为1.2g/mL)的氢氧化钠溶液和6mol/L的盐酸。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com