
题目列表(包括答案和解析)
15.匀强磁场中有一个静止的氮核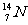 被与磁场方向垂直、速度为v的α粒子击中形成复核,然后沿与v相反方向释放出一个速度大小也v的质子,则( )
被与磁场方向垂直、速度为v的α粒子击中形成复核,然后沿与v相反方向释放出一个速度大小也v的质子,则( )
A.质子核反冲核的动能之比为17/25
B.质子核反冲核的动量大小之比为1/5
C.质子核反冲核的动量大小之比为7/18
 D.质子核反冲核在磁场中旋转的频率之比为17/8
D.质子核反冲核在磁场中旋转的频率之比为17/8
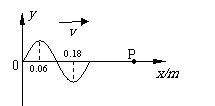
14. a、b两种色光以相同的入射角从某种介质射向真空,光路如图所示,则以下描述错误的是( )
a、b两种色光以相同的入射角从某种介质射向真空,光路如图所示,则以下描述错误的是( )
A.a光的频率大于b光的频率
B.a光在真空中的波长大于b光在真空中的波长
C.a光在介质中的传播速度大于b光在介质中的传播速度
D.如果a光能使某种金属发生光电效应,b光也一定能使该金属发生光电效应
13.科学家发现由100个碳原子构成的一个具有完美对称性的C100原子团,其中每个碳原子仍可形成四个化学键。最内部是由20个碳原子构成的正十二面体,外层的60个碳原子形成12个分立的五边形,处于中间层的碳将内外层碳原子连在一起,当它分别与氢和氟形成分子时,其分子式为( )
A.C100H20和C100F20 B.C100H60和C100F60
C.C100H112和C100F12 D.C100H40和C100F40
12.“熵”可看作是“混乱度”,它的符号是“S”。下列变化中,△S<0(“混乱度”减小)的是
A.3Fe(s)+4H2O(g)→Fe3O4(s)+4H2(g) B.2NO2(g)→N2O4(l)
C.2IBr(l)→I2(s)+Br2(g) D.(NH4)2CO3(s)→2NH3(g)+CO2(g)+2H2O(g)
11.甲、乙是两种常见的短周期元素的单质,其有关物质的转化关系如图所示,其中C为白色沉淀,D为气体,则下列说法不正确的是( )
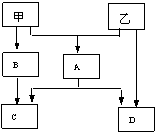 A.甲、乙两种物质生成的化合物发生水解反应不可能生成两种酸
A.甲、乙两种物质生成的化合物发生水解反应不可能生成两种酸
B.D可能为酸性气体
C.D可能为碱性气体
D.A与水反应可能生成Mg(OH)2沉淀
10.某绝热容器中有饱和石灰水,再往容器中加入少量的CaO粉末,下列判断正确的是( )
A.Ca2+的数目增加 B.c(H+)·c(OH-)的积不变
C.c(Ca2+)不变 D.c(H+)一定增大
9.有一铁的氧化物样品,用5mol·L-1盐酸100mL恰好完全溶解,所得溶液还能吸收标态的1.12L氯气,亚铁离子全部变成Fe3+,该氧化物的化学式可表示为( )
A.Fe2O3 B.Fe3O4 C.Fe4O5 D. Fe5O7
8.下列各溶液中,指定粒子的物质的量浓度关系正确的是( )
A.0.1mol·L-1硫酸铵溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-)
B.0.2mol·L-1碳酸钠溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
C.0.1mol·L-1氯化铵溶液与0.05mol·L-1氢氧化钠溶液等体积混合:
c(NH4+)+c(H+)=c(OH-)
D.0.1mol·L-1硫化钠溶液中:2c(Na+)=2c(S2-)+c(HS-)+c(H2S)
7.下列离子方程式书写正确的是( )
A.明矾溶液与氢氧化钡溶液反应,使SO42-恰好沉淀完全
Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
B.硫化氢通入醋酸铅溶液中:Pb(Ac)2+H2S=2PbS↓+2HAc
C.在暂时硬度的硬水中,加入石灰水
Ca2++Mg2++2HCO3-+2OH-=CaCO3↓+MgCO3↓+2H2O
D.Fe3O4溶于氢碘酸溶液中 Fe3O4+8H+=2Fe2++ Fe3+ +4H2O
6. 丙氨酸(CH3 CH
COOH)是一种重要的氨基酸,将其溶于水后,调节pH,测
丙氨酸(CH3 CH
COOH)是一种重要的氨基酸,将其溶于水后,调节pH,测
NH2

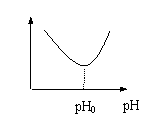 得导电能力与pH的关系如图所示。在接近中性处有一导电能力最小的点pH0,称为等电点。在等电点时,丙氨酸的主要存在形式为( )
得导电能力与pH的关系如图所示。在接近中性处有一导电能力最小的点pH0,称为等电点。在等电点时,丙氨酸的主要存在形式为( )
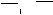
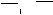 A.CH3 CH
COOH
B. CH3
CH COOH
A.CH3 CH
COOH
B. CH3
CH COOH
NH2 NH3+
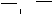
 C.CH3 CH
COO- D.CH3 CH
COO-
C.CH3 CH
COO- D.CH3 CH
COO-
NH2 NH3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com