
题目列表(包括答案和解析)
2.下列物质中同时属于纯净物、化合物、无机化合物、盐、钙盐的是
A.石灰石
B.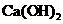 C.
C.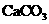 D.
D.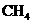
1.下列标志中,应贴在装有乙醇的容器上的是

25.(15分)现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
   |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
0.82 |
|
最高或最低化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
|
|
-3 |
-1 |
|
-3 |
|
回答下列问题:
(1)③的元素符号是 ,⑧的元素名称是 。
①在元素周期表中的位置是(周期、族) 、 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是___ ____;
碱性最强的化合物的电子式是:____ _________;
(3)比较④和⑦的氢化物的稳定性
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式
。
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式
。
24.(10分)A、B、C、D、E五种短周期元素,已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和,B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的邻族元素;D和E的原子序数之和为30。它们两两形成的化合物有甲、乙、丙、丁四种,这四种化合物中原子个数之比如下表:
|
甲 |
乙 |
丙 |
丁 |
|
A:C=1:1 |
B:A=1:4 |
D:E=1:3 |
B:E=1:4 |
(1)写出丁的化学式:
(2)写出乙的电子式:
(3)利用甲的水溶液可以处理空气中的SO2 ,并生成一种强酸。请写出该反应的化学方程式: 。
(4)向丙的水溶液中滴入NaOH溶液,直到过量,可观察到的现象是: 、
请写出相关反应的离子方程式:
(1)CCl4 (2)略(3)H2O2+SO2=H2SO4
(4)先有白色沉淀生成,后沉淀溶解;
Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O
23.(10分)A、B、C、D均为短周期元素,C与D同周期,能生成化合物CD2;C原子最外层电子数比次外层电子数的2倍还多1;D元素的族序数是其周期数的3倍;B、D两元素能组成4核42个电子的负二价阴离子; 0.1molA单质能与水反应放出氢气1.12L(标准状况);A的阳离子与D的阴离子具有相同的电子层结构,A的单质与D的单质在不同的条件下可生成A2D或A2D2。
(1)写出A、B、C、D的元素符号:A____ ___B___ _____ C_________ D________
(2)请写出A2D2的电子式:
(3)将A、B、C、D按原子半径由大到小的顺序排列(用元素符号表示): 。
(4)B、D两元素组成4核42个电子的负二价阴离子,能被氯气氧化生成两种酸根离子,且溶液呈酸性。请写出其离子方程式: 。
(1)Na、S、N、O (2)略(3)Na>S>N>O (4)SO32-+Cl2+H2O =SO42-+Cl-+2H+
22.(10分)用A+、B-、C2-、D、E、F、G和H分别表示含有10个电子的八种微粒(离子或分子),请回答:
(1)A元素是_______、B元素是_______、C元素是_______(用元素符号表示)
(2)D是由两种元素组成的双原子分子,其分子式是___________。
(3)G分子中含有4个原子,其结构式是_____________。
(1)K、Cl、S。 (2)HCl。 (3)F2。 (4) 。(5)H2O2(答PH3同样给分)。
。(5)H2O2(答PH3同样给分)。
21.(10分)(1)用电子式表示下列化合物的形成过程:
① 硫化氢
② 氟化镁
(2)填化学键类型,即离子键、极性键、非极性键
①KOH和HBr反应时形成的是
②H2+Cl2=2 HCl反应被破坏的是 形成的是
20.A、B、C、D4种短周期元素,原子序数D>A>B>C,A、B同周期,C、D同主族,A的原子结构示意图为: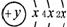 ,B、C可形成离子化合物B3C2,下列有关叙述正确的是( )
,B、C可形成离子化合物B3C2,下列有关叙述正确的是( )
A.原子半径B>A>C>D
B.原子的得电子能力:C>D>B>A
C.4种元素中D的非金属性最强
D.D和A、B同在第3周期,C和D同在ⅤA族
第Ⅱ卷(非选择题:共55分)
19.A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3:4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述中正确的是( )
A.原子序数由大到小的顺序是:D>C>B>A
B.A、B、C、D只能形成5种单质
C.按族序数由大到小的排列:C>B>A>D
D.X、Y、Z三种化合物稳定性逐渐增强
18.A、B都是短周期元素,原子半径B>A,它们可形成化合物AB2,由此可以得出的正确判断是( )
A.原子序数:A<B B.A和B可能在同一主族
C.A可能在第2周期Ⅳ A族 D.A肯定是金属元素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com